At organinių junginių reakcijos yra labai dažni ir tiriami. Verta prisiminti, kad tai yra tam tikros rūšies reakcija, kuri kaip pagrindinis ir vyraujantis mechanizmas yra nutraukti nuorodą arba nuorodas, pi kad du ar daugiau atomų galėtų pradėti būti grandinės dalimi.
Papildymo reakcijų naudojimo pavyzdys yra susijęs su margarino gamyba. Šis produktas, taip įprastas kasdieniniame žmonių gyvenime, susidaro iš augalinių aliejų hidrinimo (papildymo reakcijos) pi nuorodos jos konstitucijoje.
Papildymo reakcijų tipai yra šie:
hidrinimas (vandenilio atomų pridėjimas);
Halogeninimas (halogeno atomų pridėjimas: Cl2, br2, Aš2 ir F2);
Reakcija su halogenidu (halogeno turinčių neorganinių rūgščių, tokių kaip HCl, HI, Hbr ir HF, pridėjimas);
Drėkinimas (pridedama hidronio, H+ir hidroksilas, OH-).
Per papildymą iki hidratacija arba su halogenidu, Markovnikovo valdžia mums labai svarbu numatyti, kokie produktai bus suformuoti. Pagal šią taisyklę mes turime tą atomą hidronis (H+) į neorganinį hidroksidą ar vandenį bus įpilta
daugiau hidrintos anglies dvigubo ryšio. jau halogenas (Cl, Br, I, F) halogenido arba hidroksilas (OH-) į vandenį bus įpilta mažiau hidrintos anglies „pi“ nuorodos. Žr. Šios taisyklės taikymo pavyzdį šioje lygtyje: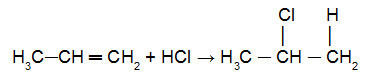
Propreno reakcija su HCl
Šioje lygtyje galime pamatyti, kad (Cl) buvo pridėta prie mažiau hidrinto anglies pi nuoroda, o atomas hidronis (H+) buvo pridėta prie labiausiai hidrinto anglies atomo pi nuoroda.
yra tik vienas išimtis į Markovnikovo taisyklę: Kharasho reakcija. Joje įvyksta inversija, tai yra atomas hidronis (H+) bus pridėta prie mažiau hidrintos anglies duoda pi nuoroda, tai halogenas (Br) halogenido bus pridėta prie daugiau hidrintos anglies duoda pi nuoroda. Išsamiau tai, kad ši reakcija įvyksta tik vienu būdu:
Nesustokite dabar... Po reklamos yra daugiau;)
Organinio peroksido buvimas;
Hbr naudojimas.
PASTABA: jei nesilaikoma šių sąlygų, Markovnikovo valdžia bus naudojami paprastai.
Toliau žr Kharasho reakcija propilene:
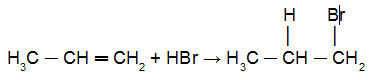
Propeno reakcija su HBr esant peroksidui
PASTABA: Verta paminėti, kad organinis peroksidas yra junginys, kurio konstitucijoje būtinai turi grupę (R─O─O─R). Kharasho reakcijose dažniausiai naudojamas organinis peroksidas gaunamas iš karboksirūgščių ir turi tokią struktūrą:
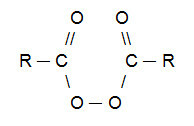
Organinio peroksido bendroji struktūrinė formulė
Kharasho reakcijos, kuria siekiama pakeisti Markovnikovo taisyklę, paaiškinimas yra tas, kad iš pradžių peroksidas suskaidomas (1 žingsnis), suformuodami laisvuosius radikalus su dviem deguonies atomais, kurie puola HBr vandenilį (2 žingsnis). Dėl šios priežasties, kuris iš pradžių puls alkeno molekulę, bus Br (3 žingsnis). Tik po to, kai vandenilis prisijungs prie alkeno grandinės. Laikykitės faktų sekos:
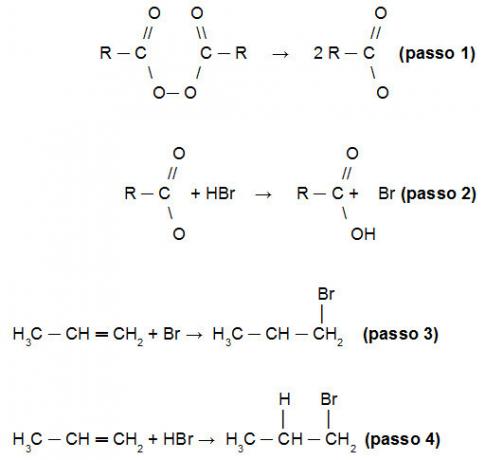
Kharasho reakcijos mechanizmo demonstravimas
Mano. Diogo Lopes Dias
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
DIENOS, Diogo Lopes. „Kharasho reakcija“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/reacao-kharash.htm. Žiūrėta 2021 m. Birželio 28 d.