Idėjos apie materijos (atomo) sandarą atsirado senovės Graikijoje, apie 450 m. a., daugiausia iš Democrito ir Leucipo. Tačiau iš tikrųjų mokslinis pobūdis atomas gavo tik po vadinamojo Daltono atominė teorija.
Daltono atominė teorija tai buvo esminis dalykas plėtojant atomo žinias, nes tai buvo pagrindas kitiems mokslininkams žinoti atomą ir jo ypatybes.
Kas buvo Johnas Daltonas?
Jonas Daltonas, baigęs chemiką, gimė Kambrijoje, Anglijoje, 1766 m., O mirė Mančesteryje 1844 m. Nuo pat mažens jo gyvenimas buvo skirtas moksliniams tyrimams ir mokymui tiek, kad jis mokė ar prisidėjo prie įvairių žinių sričių plėtojimo.
Vis dėlto didžiausias jo, kaip mokslininko, palikimas buvo pirmosios atominės teorijos sukūrimas. Būtent atlikus kelis eksperimentus, susijusius su dujų mišiniu ir žinių apie Lavoisier siūlomus darbus, 1808 metais atsirado Daltono atominė teorija.
Daltono atominės teorijos postulatai
Daltono atominė teorija buvo pagrįsta eksperimentais, tačiau nė vienas iš šių eksperimentų negalėjo aiškiai atskleisti atomo. Vadinasi, Daltonas atomą pavadino mažiausia materijos dalimi.
Daltono teorija pateikia kur kas daugiau postulatų nei įrodymų. Žiūrėkite kai kuriuos iš jų:
Atomai yra masyvūs ir sferinės formos (panašūs į biliardo kamuoliukus);
Atomai yra nedalomi;
Atomai yra nesunaikinami;
Vienas cheminis elementas tai yra tų pačių savybių (dydžio ir masės) atomų rinkinys;
Skirtingų cheminių elementų atomai turi skirtingas savybes;
Jiems diferencijuoti galima naudoti santykinį dviejų atomų svorį;
Sudėtinė cheminė medžiaga susidaro vienodai derinant skirtingų tipų atomus;
Skirtingos cheminės medžiagos susidaro sujungiant skirtingus atomus.
Daltono atominio modelio reprezentacijos
Daltonas savo atominį modelį pavadino biliardo kamuoliuku ir todėl sferiniais simboliais pradėjo atstovauti jo laikais žinomų elementų atomus.
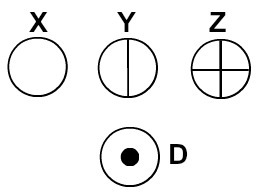
Atomai, vaizduojami pagal Daltono atominę teoriją
Kiekvienas atomo atvaizdavimas, turintis tam tikrą detalę, nurodo skirtingą cheminį elementą. Didaktiškai pradinio ir vidurinio lygio knygos ir pratimai atomus vaizduoja tik skirtingų spalvų sferomis.
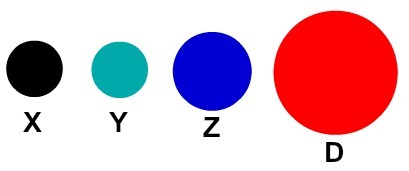
Didaktinis atomų vaizdavimas
Daltono atominės teorijos indėlis
supratimas Lavoisierio mišių išsaugojimo įstatymas
Prancūzų chemikas Lavoisier 1785 metais teigė, kad „Vykstant cheminei reakcijai, masė išsaugoma, nes nėra nei atomų sukūrimo, nei sunaikinimo ”. Daltono atominė teorija įrodė šį faktą, nes vienas iš jo postulatų teigia, kad atomas yra nesunaikinamas.
Todėl jei vykdysime anglies (C) deginimą esant deguonies dujoms (O2), turėsime cheminę reakciją tarp vieno anglies atomo ir dviejų deguonies atomų. Šios reakcijos metu susidarys anglies dioksidas (CO2), kuriame yra lygiai tie patys atomai, kurie sudarė medžiagas prieš reakciją.
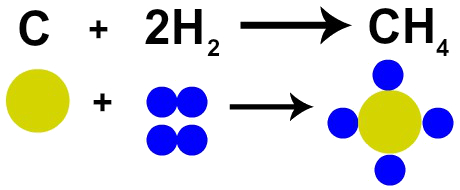
Lavoisierio įstatymo atvaizdavimas pagal Daltono atominį modelį
supratimas paprastos medžiagos
Naudojant Daltono atominis modelis, mes galime suprasti paprastą medžiagą, tai yra, turinčią tos pačios charakteristikos atomus, formuojančius molekulę. Todėl mes turime atomus, priklausančius tam pačiam cheminiam elementui.
F medžiagoje2, pavyzdžiui, mes turime du fluoro atomus, todėl vaizduodami pagal Daltono atominę teoriją turime naudoti dviejų tipų vienodus atomus.

Paprastas medžiagos atvaizdavimas pagal Daltono atominis modelis
supratimas sudėtinės medžiagos
Sudėtinėje medžiagoje molekulę sudaro skirtingų savybių atomai. Todėl mes turime skirtingus cheminius elementus, formuojančius medžiagą.
Medžiaga H2Pavyzdžiui, O turi tris atomus: du vandenilį ir vieną deguonį. Žiūrėkite jo atvaizdavimą pagal atominį Daltono modelį:
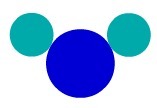
Sudėtinės medžiagos atvaizdavimas pagal odąDaltono atominis modelis
Mišinių supratimas
Mišinio (dviejų ar daugiau skirtingų medžiagų susijungimo) supratimas per Daltono atominę teoriją yra paprastas: tiesiog įdėkite dvi skirtingas molekules į tą patį indą.

Antrojo mišinio vaizdavimas Daltono atominis modelis
Kiti Johno Daltono moksliniai darbai
pristatė atominė masė;
Suformulavo dujų dalinio slėgio dėsnį (Daltono įstatymas);
Atrado vadinamą regėjimo negalią spalvų aklumas;
Tirta garų ir dujų elgsena esant skirtingoms temperatūroms;
Jis nustatė, kad visos dujos vienodai plečiasi (jie bando užimti tam tikrą vietą) erdvėje.
Mano. Diogo Lopes Dias
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm

