Vienas iš didžiausių iššūkių tiems, kurie mokosi chemijos, vadinamas elektroniniu platinimu. Tai, ką pateiksime šiame kontekste, gali labai palengvinti jūsų tyrimus, susijusius su mokslininko Linuso Paulingo pasiūlyta elektronų konfigūracija.
Didžiausias elektronų skaičius, tinkantis kiekvienam sluoksniui ar energijos lygiui, nurodytas lentelėje:
Energijos lygio sluoksnis Didžiausias elektronų skaičius
1-asis K 2
2-asis L 8
3-asis M 18
4 N 32
5 ° O 32
6-asis P 18
7-asis Q 8
Didėjanti pakopų energijos tvarka yra tvarka įstrižainių sekoje. Linus Pauling diagrama parodyta žemiau:
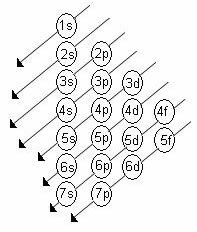
Pagrindinės taisyklės:
1. Atominis elemento (Z) skaičius neutralioje būsenoje nurodo pasiskirstančių elektronų skaičių. Šis skaičius pavaizduotas apatinėje kairėje elemento simbolio dalyje.
2. Naudodamiesi Paulingo diagrama, pradėkite paskirstyti elektronus iš viršaus į apačią, atsižvelgdami į didėjančią energijos tvarką (nukreiptą rodyklių kryptimi).
3. Užpildykite potipius maksimaliu elektronų lygiu. Jei nurodytame potinkyje yra tik 6 elektronai, neviršykite šios sumos.
4. Patikrinkite elektronų skaičių, sudėdami juos į kiekvieną pakopą.
Panaudokime tai praktiškai?
Paskirstykite geležies atomo elektronus (Z = 26).
Jei atomo skaičius yra 26, tai reiškia, kad normaliame geležies atome yra 26 elektronai. Taikydami Paulingo diagramą, turėsime:

Autorius Líria Alves
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm
