Kadangi organinių junginių yra tūkstančiai, izomerizmo reiškinys gali būti kelių formų. Todėl izomerizmą iš esmės galima suskirstyti į du tipus: plokščias ar konstitucinis izomerizmas ir kosmoso izomerija arba stereoizomerija. Kiekvieną paminėtą tipą galima suskirstyti, kaip parodyta šioje diagramoje:
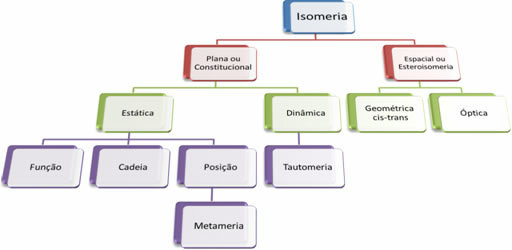
Žr. Kiekvieną atvejį:
1. Plokščias ar konstitucinis izomerizmas: Šio tipo izomerai turi tą pačią molekulinę formulę ir skiriasi plokščiomis struktūrinėmis formulėmis. Yra penki plokštuminės izomerijos atvejai: funkcija, grandinė, padėtis, metamerizmas ir tautomerizmas.
1.1.Funkcinis arba funkcinis izomerizmas: Skirtumas tarp izomerų yra funkcinėje grupėje.
Pavyzdys: molekulinė formulė C3H6O
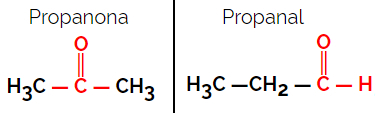
Atkreipkite dėmesį, kad propanonas yra iš ketonų grupės, o propanalas - iš aldehido grupės.
1.2. Grandinės ar griaučių izomerai: Izomerų skirtumas yra grandinės tipas. Pvz., Vienas izomeras yra atviros grandinės, o kitas - uždaros grandinės, arba vienas yra normalios, o kitos šakotos grandinės, arba vienas yra homogeninė grandinė, o kitas yra heterogeninė grandinė.
Pavyzdys: molekulinė formulė C4H10
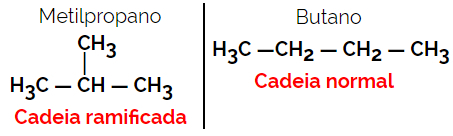
1.3.Padėties ar padėties izomerija: Skirtumas yra nesočiųjų, funkcinių grupių, heteroatomų ar pakaitų padėtyje.
Pavyzdys: molekulinė formulė C4H6

1.4.Kompensacinė izomerija arba metamery: Tai yra specialus padėties izomerizmo tipas, kur skirtumas yra heteroatomo padėtis.
Pavyzdys: molekulinė formulė C4H10O
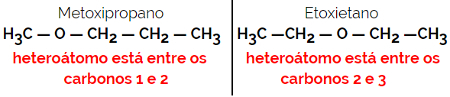
1.5.Dinaminė izomerija arba tautomerija: Tai yra ypatingas funkcinės izomerijos tipas, kai izomerai egzistuoja dinaminėje pusiausvyroje tirpale. Du pagrindiniai tautomerijų tipai yra tarp ketono ir enolio (ketoenolio balansas) ir tarp aldehido ir enolio (aldoenolio balansas).
Pavyzdys: molekulinė formulė C3H6O
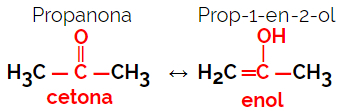
2. Kosmoso izomerija arba steroisomerija: Šiuo atveju skirtumas tarp izomerų gali būti vizualizuojamas tik per jų atomų orientaciją erdvėje. Yra du stereoizomerizmo tipai: geometrinis izomerizmas ir optinis izomerizmas.
2.1.Geometriniai arba cis-trans izomerai: Skirtumas tas, kad izomeras vadinamas cis jis turi tuos pačius anglies ligandus dviguboje jungtyje arba cikliniuose junginiuose toje pačioje plokštumos pusėje. Izomeriniai ligandai vert yra priešingose pusėse.
Pavyzdys: molekulinė formulė C2H2Cl2

Šie junginiai vadinami stereoizomerai.
2.2.Optinis izomeras: Atsiranda, kai izomerai sugeba nukreipti poliarizuotos šviesos pluoštą. Jei jis lenkia poliarizuotą šviesos pluoštą į kairę, tai yra levorotarinis izomeras, bet jei jis lenkiasi į dešinę, jis vadinamas dešiniarankiu izomeru.
Pavyzdys:
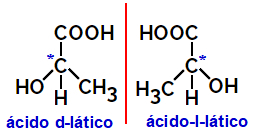
Asimetrinės molekulės, panašios į aukščiau pavaizduotas, kurios yra veidrodiniai vienas kito vaizdai ir kurios nėra uždėtos, vadinamos enantiomerai.
Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/tipos-isomeria.htm
