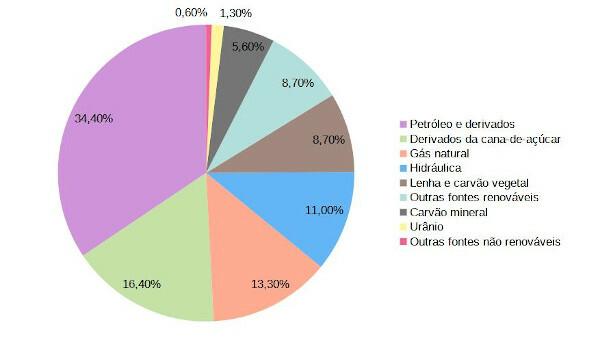
Paprastai reakcijos vandeninė elektrolizė ir magminė elektrolizė jie atliekami su grafito ir platinos elektrodais, kurie nedalyvauja reakcijoje; jie praleidžia tik elektros srovę. Tačiau yra keletas konkrečių atvejų, kai tai būtina naudoti aktyvūs elektrodai, tai yra, kurie patiria redukciją ir oksidaciją.
Pagrindiniai šių elektrodų, dalyvaujančių redokso procese, naudojimo atvejai yra šie: a elektrolitinis metalo valymas, tokių kaip cinkas, kobaltas, nikelis ir daugiausia varis; ir taip pat galvanizavimas. Pažiūrėkime, kaip įvyksta kiekvienas atvejis:
• Vario elektrolitinis gryninimas: šis elektrolitinis vario rafinavimas gali sukelti maždaug 99,9% grynumą ir daugiausia naudojamas gaminti variniai laidai, kurie, jei turi mažiausiai priemaišų, gali praleisti labai elektros srovę sumažėjo.
Stebėkite, kaip vyksta šis procesas, matydami žemiau surinktos elektrolitinės talpos schemą:

Vario sulfato vandeniniam tirpalui (CuSo4 (aq)) - kuris praleidžia elektrą - taip, kad anodas, kuris yra nešvarus metalinis varis, praranda elektronus, tai yra oksiduojasi, išlaisvindamas katijonus (
2+), kurie nusėda ant neigiamos plokštelės. Tai gali būti inertiška platinos plokštė arba, geriau, gryno vario plokštė. Jis sudaro katodą, kuris redukuojamas, kai jame kaupiasi varis. Taigi elektroduose vykstančios pusiau reakcijos yra: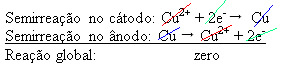
Tai, kad rezultatas buvo lygus nuliui, rodo, kad nebuvo jokios cheminės reakcijos, o tik vario transportas. Talpyklos dugne yra kitos vario turinčios nešvarios medžiagos, tokios kaip auksas, sidabras, silicio dioksidas (smėlis) ir kiti mineralai, kuriuos galima net parduoti.
• Galvaninis dengimas: metalinė danga padengiama medžiaga, kuri turi būti apsaugota nuo korozijos.
Dangai pasirinktas metalas, kuris gali būti chromas (chromas), nikelis (nikelis), sidabras (sidabras), auksas (paauksavimas) arba cinkas (cinkavimas) - bus anodas, teigiamas elektrodas, kuris patiria oksidaciją, praranda elektronus. Vietoj saugomos medžiagos jis oksiduojasi, nes jo redukcijos potencialas yra didesnis.
Neigiamas elektrodas, tai yra katodas, priimantis šiuos elektronus ir patyręs redukciją, yra pati medžiaga, kuri buvo padengta. Tokiu būdu jis lieka apsaugotas, net jei jo paviršius yra kažkaip pažeistas.
Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm