Apsvarstykite toliau pateiktą bendrą grįžtamąją reakciją, kur mažosios raidės atitinka subalansuotus reakcijos koeficientus, o didžiosios raidės yra reagentai, o visi produktai yra dujiniai:

Atsižvelgiant į kiekvieną reakcijos kryptį atskirai, jų vystymosi tempus (Td) pateikia:
* Tiesioginė reakcija: aA + bB → cC + dD
Viskastiesioginis = Ktiesioginis. [THE]The. [B]B
* Atvirkštinė reakcija: cC + dD → aA + bB
Viskasatvirkštinis = Katvirkščiai. [Ç]ç. [D]d
Cheminės pusiausvyros konstanta pagal medžiagos kiekio koncentraciją (Kç) ir dalinio slėgio atžvilgiu (KP) bus duodama dalijant Ktiesioginis pateikė Katvirkščiai.
Taigi mes turime:
K.tiesioginis. [THE]The. [B]B = 1 → K.tiesioginis__ = __[Ç]ç. [D]d___
K.atvirkščiai. [Ç]ç. [D]d K.atvirkščiai [THE]The. [B]B
Būdamas, K.ç =_Ktiesioginis_
K.atvirkščiai
Taigi mes turime:
K.ç =__[Ç]ç. [D]d___ arba K.P =__(Praça)ç. (pD)d___ |
Kur p yra kiekvienos medžiagos pusiausvyros slėgis.
Tokiu būdu kiekviena koncentracija pakeliama iki eksponento, atitinkančio atitinkamos medžiagos reakcijoje koeficientą, ir Kç neturi vieneto *.
Be to, labai svarbus aspektas, kurį reikia pabrėžti, yra tai, kad šioje išraiškojeneturėtų būti vaizduojami nei kietieji komponentai, nei gryni skysčiai., nes šioje išraiškoje dalyvauja tik tie dalykai, kurie gali nukentėti. Medžiagos koncentracija kietoje būsenoje yra pastovi ir todėl jau yra įtraukta į pačios K vertę.ç. Tas pats pasakytina apie grynus skysčius, tokius kaip vanduo. Trumpai tariant, ekspresijoje dalyvauja tik dujinės būsenos ir vandeninio tirpalo medžiagos.
Atkreipkite dėmesį į toliau pateiktus pavyzdžius:
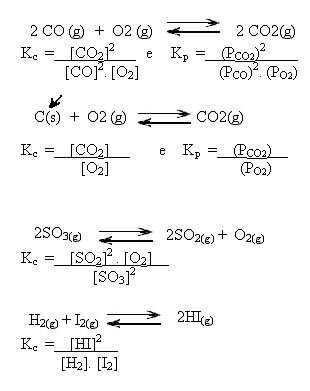
K reikšmėsç gali parodyti, ar reagentų ir produktų koncentracija yra vienoda, ar viena yra didesnė už kitą:
- jei K.ç arba K.P yra lygus vienam (Kç = 1), tai reiškia, kad reagentų ir produktų koncentracija yra vienoda;
- Jei vertė K.ç arba K.P būti aukštas, tai reiškia, kad produktai yra didesnės koncentracijos, nes išreiškiant Kç produktai yra skaitiklyje;
- Jei vertė K.ç arba K.P yra žemas, tai reiškia, kad reagentų koncentracija yra didesnė, nes išreiškiant Kç reagentai yra vardiklyje.
* K.ç ir K.P jie yra be matmenų skaičiai, tai yra gryni skaičiai, be vieneto, susijusio su jokiu dydžiu ar santykiu tarp dydžių.
Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm
