THE oganessonas, simbolis Og, atominis skaičius 118, yra cheminis elementas, kurio atominis skaičius iki šiol yra didžiausias periodinėje lentelėje. Gamtoje jo negalima rasti, o jo gamyba yra dirbtinė, todėl laikoma sintetiniu elementu. Nepaisant to, jo gamyba yra labai sudėtinga ir laikomas labai retu elementu, kuris buvo susintetintas labai nedaug kartų.
Nepaisant to, kad priklauso tai pačiai grupei kaip tauriųjų dujųRemiantis skaičiavimais, oganessonas neturi daug charakteristikų, susijusių su šiais elementais Matematikai įrodo, kad dėl reliatyvistinių efektų kenčia itin sunkūs elementai.
Elementas 118 pirmą kartą buvo susintetintas 2002 m., vykstant jonų reakcijai 48Ca su atomais 249Pamatyti Jo pavadinimas yra duoklė rusų mokslininkui Jurijui Oganessianui, vienam iš labiausiai gerbiamų ir pripažintų itin sunkiųjų elementų srityje.
Taip pat žiūrėkite: Rutherfordium – sintetinis cheminis elementas, pavadintas mokslininko Ernesto Rutherfordo vardu
Santrauka apie oganesson
Oganessonas yra sintetinis cheminis elementas, priklausantis 18 grupei Periodinė elementų lentelė.
Pirmą kartą jis buvo susintetintas 2002 m., bendrame Rusijos ir Amerikos mokslininkų darbe.
Ji sudaro elementų grupę, kuri neseniai, 2016 m., buvo įtraukta į periodinę lentelę.
Tai labai retas elementas, susintetintas labai nedaug kartų.
Jų tyrimai dar labai neseni, o pagrindinės savybės vis dar nustatomos skaičiavimais ir matematiniais modeliais.
Preliminarūs teoriniai bandymai rodo, kad, nepaisant priklausymo inertinių dujų grupei, kai kurios savybės nutolina Og nuo kitų elementų.
Oganessono gamyba vyksta iki Branduolinė sintezė, naudojant jonus 48Ca ir atomai 249Pamatyti
Jo pavadinimas yra duoklė rusų mokslininkui Jurijui Oganessianui, vienam svarbiausių supersunkiųjų elementų tyrimo srityje.
oganessono savybės
Simbolis: Oi
Atominis skaičius: 118.
Atominė masė: 294 c.u. (neoficiali Iupac).
Elektroninė konfigūracija: [Rn] 7s2 5f14 6d10 7p6.
Stabiliausias izotopas: 294Og (0,69 milisekundės pusinės eliminacijos laikas, kurį galima padidinti 0,64 milisekundės arba sumažinti 0,22 milisekundės).
Cheminė serija: 18 grupė, supersunkieji elementai, tauriosios dujos.
Oganessono savybės
Oganessonas yra iki šiol oficialiai paskelbtas didžiausio atominio skaičiaus elementas (118). Tarptautinės grynosios ir taikomosios chemijos sąjungos (IUPAC). Nors pirmą kartą jis buvo pagamintas 2002 m. apie jį mažai žinoma. Dar daug spėliojama, nes šio elemento gamtoje nėra. Jo gamyba atliekama laboratorijoje, kuri sukonfigūruoja jį kaip sintetinį elementą.
Be to, tavo pusė gyvenimo yra mažiau nei milisekundė (10-3 antroji) – prisiminti, kad pusinės eliminacijos laikas yra laikas, kurio reikia, kad kiekis sumažėtų perpus. Todėl šio elemento savybės yra ne kas kita, kaip rezultatai teoriniai skaičiavimai, pagrįsti matematiniais modeliais, nes periodinės lentelės srityje, kurioje ji yra randa reliatyvistiniai efektai (tikėtino ir pastebėto poveikio neatitikimas dėl reliatyvumo) yra reikšmingi.
Reliatyvistiniai efektai atima Ogą nuo to, ko iš jo buvo tikimasi. Elementas, pvz. nepasižymi panašiu elgesiu kaip tauriosios dujos. Skaičiavimai rodo, kad oganessonas būtų kietas kambario temperatūroje, kurio lydymosi temperatūra 325 ± 15 K (apie 52 °C) ir virimo temperatūra 450 ± 10 K (apie 177 °C).
Taip pat žinoma, kad Og gali būti reaktyvesnis nei kitos tauriosios dujos, nes reliatyvistiniai efektai leidžia lengviau prarasti p-sublygio elektronus. Kitas nesutarimų su tauriosiomis dujomis dalykas yra tas, kad oganessonas yra a puslaidininkis, o kiti yra izoliatoriai.
Taip pat skaitykite: Vandenilis – cheminis elementas, kurio atominis skaičius periodinėje lentelėje yra mažiausias
Oganessono gavimas
Kaip ir kiti itin sunkūs elementai, oganessonas gaunamas naudojant techniką, vadinamą karštas lydalas, kur izotopo jonai 48Ca, randamas natūraliai, bet labai mažai prieinamas, reaguoja su daug sunkesniais izotopais, kad susidarytų itin sunkūs elementai.
Og yra toks retas ir sunkiai gaunamas elementas, kad Per dešimties metų laikotarpį tik ketveri atomai atėjo gaminti. Iš esmės, gamyba 294Og, vienintelis žinomas izotopas, atsiranda bombarduojant jonus 48Ca iki šerdies 249Plg. su 3 neutronų išsiskyrimu.
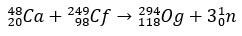
Kai pusinės eliminacijos laikas yra kelios milisekundės, Og buvo identifikuotas pagal jo irimo modelį, tai labai įprasta itin sunkiems elementams. Šiuo atveju įvyko 3 alfa skilimas, dėl kurio elementas 118 tapo koperniciu Cn, kuris galiausiai spontaniškai dalijo.
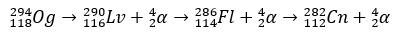
oganessono istorija
Pirmoji oganessono sintezė įvyko 2002 m., Livermore mieste, Kalifornijoje, Jungtinėse Amerikos Valstijose, Lawrence Livermore nacionalinėje laboratorijoje, kur grupė amerikiečių mokslininkų bendradarbiavo su Rusijos tyrinėtojais garsaus Jungtinio branduolinių tyrimų instituto (JINR), vadovaujamo rusų mokslininko Jurijaus Oganessiano.
Per dešimt metų nuo pirmosios sintezės buvo susintetinti tik keturi oganessono atomai dėl reakcijos parametrų retumo ir sudėtingumo. Tačiau ketvirtasis ir paskutinis atomas pateikė neįtikėtiną atradimą.
Mokslininkai bandė susintetinti elementą 117 per reakciją 48Ca su 249Bk, tačiau buvo pastebėta, kad 28% berkelio taikinio patyrė β skilimą, paverčiant 249Žr. ir taip sukuriamas elementas 118. Pažymėtina, kad elemento 118 pavadinimas pagerbiamas rusų mokslininkas Jurijus Oganessianas, duoklė gyviems chemikams chemijos istorijoje įvyko tik du kartus, pirmiausia Glennui Seaborgui su Seaborgium.
Išsprendė pratimus ant oganessono
Klausimas 1
Oganessonas, elementas su atominiu numeriu 118 ir simboliu Og, buvo įtrauktas į septintą periodinės lentelės periodą, į tauriųjų dujų grupę. Dėl to daug buvo spėliojama, ar toks elementas pasižymi dideliu stabilumu, o tai yra žinoma kitiems šios grupės elementams. Og priskyrimas 18 grupei įvyko dėl:
A) šis elementas yra labai stabilus.
B) šio elemento valentiniame apvalkale yra aštuoni elektronai.
C) šis elementas kambario temperatūroje akivaizdžiai yra dujos.
D) šis elementas turi tas pačias chemines savybes kaip ir kitos tauriosios dujos.
E) šis elementas turi didelę jonizacijos energiją.
Rezoliucija:
Alternatyva B
Og paskirstymas vyksta tik ir išimtinai dėl jo elektroninis platinimas. Faktas, kad jame yra aštuoni elektronai valentinis sluoksnis, 7s2 7p6, pastato jį į tokią padėtį. Tyrimai su šiuo elementu vis dar yra preliminarūs, tačiau dėl matematinių rezultatų jau spėjama, kad, pavyzdžiui, Og nėra dujos kambario temperatūroje. Kitas dalykas, kurį reikia pabrėžti, yra tai, kad Og nėra stabilus, net neegzistuoja gamtoje.
2 klausimas
Dėl didelių sunkumų gaminant 118 elementą kyla mintis, kad mokslininkai, siekdami jį aptikti, ėjo tikra odisėja. Nenuostabu, kad po dešimties metų pirmosios sintezės oganessonas buvo susintetintas tik tris kitus kartus. Ir iki šiol žinomas tik vienas izotopas, 294Oi Kiek neutronų turi žinomas oganessono izotopas?
A) 294.
B) 118.
C) 176.
D) 412.
E) 166.
Rezoliucija:
Alternatyva C
Skaičius neutronų Og galima apskaičiuoti taip:
A = Z + n
A yra skaičius makaronai atominis, Z yra protonų skaičius (arba atominis skaičius), o n yra neutronų skaičius. Pakeitę vertes, turime:
294 = 118 + n
n = 294–118
n = 176
Autorius Stefano Araújo Novais
Chemijos mokytojas
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/oganessonio-og.htm
