THE teneso (arba teneso), simbolis Ts, yra elementas numerį atominis 117 periodinės lentelės. Jo atradimas buvo visai neseniai, 2009 m., o į periodinę lentelę įtrauktas tik 2015 m. pabaigoje. Gamtoje jo nerandama jokiu izotopu, todėl jis turi būti gaminamas laboratorijoje, nes yra sintetinis cheminis elementas.
Tenneso savybės vis dar tiriamos taikant teorinę chemiją ir matematinius skaičiavimus, atsižvelgiant į mažą gamybos greitį. Jo gamyba vyksta per reakciją tarp 48Ca ir 249Bk, kad būtų galima pagaminti 294 arba 293 elemento izotopą.
Pavadinimas nurodo JAV Tenesio valstiją, kai kurių mokslininkų, dalyvaujančių atrandant ir gaminant izotopą, kilmės vietą. 249Bk, toks svarbus šio naujo elemento sintezei.
Taip pat žiūrėkite: Bohrium - dar vienas sintetinis cheminis elementas, kurio gamybos greitis yra mažas
Tenneso santrauka
Tenesso yra sintetinis cheminis elementas, priklausantis 17 grupei Periodinė elementų lentelė.
Pirmą kartą jis buvo susintetintas 2009 m., bendrame Rusijos ir Amerikos mokslininkų darbe.
Tai nepriklausomai patvirtino vokiečių mokslininkai.
Ji sudaro elementų grupę, kuri neseniai, 2016 m., buvo įtraukta į periodinę lentelę.
Jų tyrimai dar labai neseni, o jų savybės nustatomos matematiniais metodais.
Jo gamyba yra Branduolinė sintezė, naudojant jonus 48Ca ir atomai 249bk.
Jos pavadinimas reiškia JAV Tenesio valstiją.
Nesustok dabar... Po skelbimo yra daugiau ;)
Teneso savybės
Simbolis: Ts.
Atominis skaičius: 117.
Atominė masė: 293 c.u. arba 294 c.u. (neoficialus „Iupac“).
Elektroninė konfigūracija: [Rn] 7s2 5f14 6d10 7p5.
Stabiliausias izotopas:294Ts (51 milisekundė pusė gyvenimo, kuris gali skirtis 38 milisekundėmis daugiau arba 16 milisekundžių mažiau).
Cheminė serija: 17 grupė, halogenai, supersunkieji elementai.
Tenesso savybės
Tenesas (arba tenesas), simbolis Ts, buvo vienas iš paskutinių keturių elementų, kuris turi būti oficialiai paskelbtas Tarptautinė grynosios ir taikomosios chemijos sąjunga (IUPAC) savo periodinėje lentelėje. Turėdamas atominį numerį 117, jis yra 17 grupėje halogenai.
Pirmą kartą jis buvo pagamintas 2009–2010 m, tačiau „Iupac“ jį patvirtino tik 2015 m. gruodžio 30 d. Tokio dydžio atominio skaičiaus ir skaičiaus elementai neutronų gamtoje nėra randami ir turi būti sukurti laboratorijoje, todėl tai yra a sintetinis cheminis elementas.
Pagrindinė priežastis, kodėl jie nerandami gamtoje, yra tai, kad jie yra labai nestabilūs. Kai jie gaminami per branduolines reakcijas, jie patiria radioaktyvus skilimas per kelias sekundes (kartais mažiau, milisekundžių diapazone).
Be to, tokie elementai kaip Ts gaminami lėtai, su mažas derlius. Konkrečiai tenesso atveju mokslininkai reakciją palaikė 70 dienų, kad aptiktų šešis šio elemento atomus.
Todėl šiuo metu mokslininkai teoriniais skaičiavimais ir matematiniais modeliais bando nustatyti pagrindines Ts ir kai kurių jo junginių savybes. Atliktame ir paskelbtame tyrime Cheminės fizikos laiškai, Brazilijos mokslininkas Robsonas Fernandesas de Farias įvertino kai kurias fizines Ts savybes ir tennesso, TsH, pvz., kovalentinis spindulys, poliarizuotumas, kovalentinio ryšio atstumas, taip pat ryšio energija kovalentinis.
Žinoti daugiau: Oganessonas – cheminis elementas, kurio atominis skaičius yra didžiausias periodinėje lentelėje
gauti teneso
Itin sunkūs elementai, tokie kaip teneso, gaunami naudojant techniką, vadinamą karštos sintezės reakcija (nemokamas vertimas iš karštos sintezės reakcija). Šioje technikoje įprasta naudoti jonus 48Ca, stabilus izotopas kalcio, kurio natūralus 0,2 % gausumas ir aštuoniais neutronais daugiau nei įprastinio izotopo.
Dėl Ts – jonai 48Ca reagavo su izotopu 249Bk, aktinidas. Taigi, iš pradžių, 297Ts, kurie greitai suskyla ir prarado tris ar keturis neutronus, sudarydami izotopus 294Ts ir 293Ts.
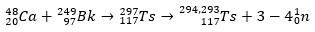
Visa tai buvo galima patikrinti naudojant α skilimo grandinių analizė, kuris pasiekė dubnium ir rentgenas. Kadangi gauti Ts izotopai yra nestabilūs, jie spontaniškai patiria α skilimo reakcijas arba tai yra, jie išskiria α dalelę (kuri turi du protonus ir du neutronus), kol pasiekia stabilius branduolius.
Suirimo pėdsaku mokslininkai sugebėjo sudėti dėlionę ir taip patvirtinti itin sunkaus elemento egzistavimą. izotopui 293Ts, buvo trys α skilimai iki 281Rg, o izotopui 294Ts buvo šeši α skilimai iki 270DB
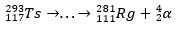
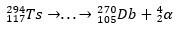
teneso istorija
117 elementas, pirmą kartą, buvo sukurtas per platų tarptautinį Rusijos ir Amerikos mokslininkų bendradarbiavimą, kuris vyko Flerovo branduolinių reakcijų laboratorijos (FLNR), esančios Jungtiniame branduolinių tyrimų institute, Dubnos mieste, Rusijoje, patalpose.
Pažymėtina, kad nepriklausomai, rezultatus dar patvirtino vokiečių mokslininkai iš Helmhotzo sunkiųjų jonų tyrimų centro (GSI), esančio Darmštate, Vokietijoje. Per 70 dienų, 2009 m., FLNR mokslininkų komanda reagavo į jonus 48Ca su atomais 249Bk taip gauti šešis 117 elemento atomus. Tada, 2012 m., mokslininkams pavyko gauti septynis 117 elemento atomus.
Nepriklausomas GSI patvirtinimas įvyko dėl kito bandymo: mokslininkai bandė sukurti elementą 119, kuris atvertų aštuntą periodinės lentelės periodą. Šiuo atveju idėja buvo reaguoti į joną 50Tave su taikiniu 249bk. Tačiau, nepaisant pastangų, šis elementas nebuvo aptiktas po keturių mėnesių bandymų.
Titano jonų keitimas 48Ca, GSI mokslininkai ieškojo reto, bet žinomo itin sunkaus elemento, norėdami patikrinti savo eksperimentines procedūras. Taigi jie susintetino elementą 117, kuris padėjo šį elementą patvirtinti Iupac.
THE Teneso pavadinimas yra nuoroda į JAV Tenesio valstiją.Tai buvo būdas ne tik pagerbti kai kurių mokslininkų, dalyvavusių FLNR eksperimentuose, kilmę, bet ir prisiminti vietą, kur buvo rasti FLNR izotopai. 249Bk, tokie svarbūs atradimui, buvo susintetinti, kai buvo gaminami Oak Ridge nacionalinėje laboratorijoje. Anglų kalba elemento pavadinimas yra tenesinas, kurio galūnė yra kartu su kitais halogenais: fluoras, chloro, bromas, jodo, ir astatinas.
Išsprendė teneso pratimus
Klausimas 1
Tenesso, simbolis Ts, yra elementas, kuris vėliausiai įtrauktas į halogenų grupę (17 grupė). Todėl tikimasi, kad, remiantis periodinėmis savybėmis, jo cheminė elgsena yra panaši į šios grupės elementų. Taigi tarp šių alternatyvų galima teigti, kad teneso:
A) turi šešis valentinius elektronus.
B) turi mažiausią atominį spindulį tarp šios grupės elementų.
C) turi mažiausią elektronegatyvumą tarp šios grupės elementų.
D), norint pasiekti visą oktetą, reikia trijų elektronų.
E) turi didžiausią 17 grupės elektronų afinitetą.
Rezoliucija:
Alternatyva C
Ts, kaip ir visi 17 grupės elementai, turi septynis elektronus valentinis sluoksnis, turintis valentinį sluoksnį 7s2 7p5. Taigi galima daryti išvadą, kad oktetui pasiekti jam reikėtų elektrono, nes jo valentiniame apvalkale yra septyni elektronai.
Kaip elementas, turintis daugiausia elektronų apvalkalų tarp halogenų, Ts taip pat turi didžiausią atominis spindulys, kuri garantuoja mažiau elektronų giminingumas, nes pridėti elektronai būtų gana toli nuo branduolio. Mažiausias spindulys taip pat lemia, kad teneso elektronegatyvumas yra mažiausias iš visų 17 grupės elementų.
2 klausimas
Teneso, simbolis Ts ir atominis skaičius 117, pirmą kartą buvo aptiktas susidarius dviem jo izotopams: masė 293 ir masė 294. Taigi galima teigti, kad neutronų skaičius 293Ts ir nuo 294Ts yra atitinkamai lygus:
A) 293 ir 294
B) 117 ir 118
C) 177 ir 294
D) 176 ir 177
E) 176 ir 293
Rezoliucija:
Alternatyva D
Dviejų izotopų neutronų skaičių galima nustatyti taip:
A = Z + n
A yra skaičius makaronai atominis, Z protonų skaičius (atominis skaičius), o n yra neutronų skaičius.
Pakeitę 293 izotopą, turime:
293 = 117 + n
n = 293–117
n = 176
Izotopui 294 turime:
294 = 117 + n
n = 294–117
n = 177
Autorius Stefano Araújo Novais
Chemijos mokytojas

