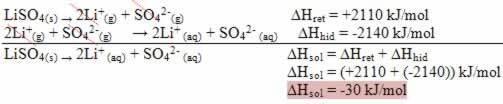
Periodinė elementų lentelė yra modelis, kuris grupuoja visus žinomus cheminius elementus ir jų savybes. Jie yra išdėstyti didėjančia atominių skaičių (protonų skaičiaus) tvarka.
Iš viso naujojoje periodinėje lentelėje yra 118 cheminių elementų (92 natūralūs ir 26 dirbtiniai).
Kiekviename kvadrate nurodomas cheminio elemento pavadinimas, jo simbolis ir jo atomo numeris.
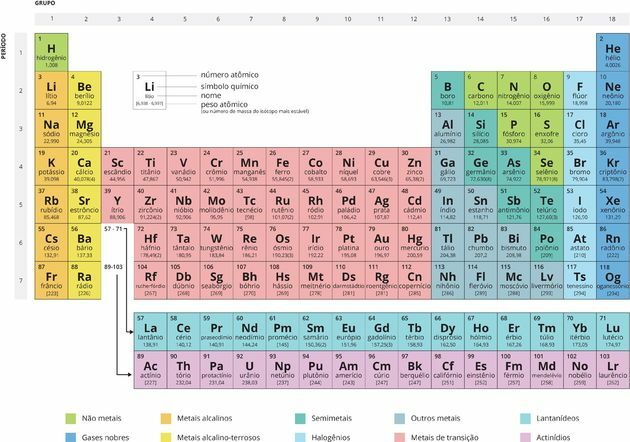
Periodinių lentelių organizavimas
skambučių Laikotarpiai jie yra sunumeruotos horizontalios linijos, turinčios elementų, turinčių tą patį elektroninių sluoksnių skaičių, iš viso septynis periodus.
- 1-asis laikotarpis: 2 elementai
- 2-asis laikotarpis: 8 elementai
- 3-asis laikotarpis: 8 elementai
- 4-asis laikotarpis: 18 elementų
- 5-asis laikotarpis: 18 elementų
- 6-asis laikotarpis: 32 elementai
- 7-asis laikotarpis: 32 elementai
Organizuojant lentelėje esančius laikotarpius, kai kurios horizontalios linijos taptų labai ilgos, todėl įprasta lantanido ir aktinido serijas vaizduoti atskirai nuo kitų.
At Šeimos arba grupės yra vertikalios kolonos, kur elementai turi tą patį elektronų skaičių tolimiausiame apvalkale, tai yra
valentinis sluoksnis. Daugelis šių grupių elementų yra susiję pagal jų grupes cheminės savybės.Yra aštuoniolika grupių (A ir B), o žinomiausios šeimos yra iš A grupės, taip pat vadinamos reprezentatyvūs elementai:
- 1A Šeima: Šarminiai metalai (ličio, natrio, kalio, rubidžio, cezio ir frankio).
- 2A Šeima: Šarminiai žemės metalai (berilis, magnis, kalcis, stroncis, baris ir radis).
- 3A Šeima: Boro šeima (boras, aliuminis, galis, indis, talis ir nihonis).
- 4A Šeima: Anglies šeima (anglis, silicis, germanis, alavas, švinas ir flerovas).
- 5A Šeima: Azoto šeima (azotas, fosforas, arsenas, stibis, bismutas ir muskusas).
- 6A Šeima: Chalkogenai (deguonis, siera, selenas, telūras, polonis, livermoris).
- 7A Šeima: Halogenai (fluoras, chloras, bromas, jodas, astatinas ir tenessinas).
- 8A Šeima: Tauriosios dujos (Helis, Neonas, Argonas, Kriptonas, Ksenonas, Radonas ir Oganessoniumas).
Tu perėjimo elementai, dar vadinami pereinamaisiais metalais, atstovauja 8 B grupės šeimoms:
- 1B šeima: varis, sidabras, auksas ir roženas.
- 2B šeima: cinkas, kadmis, gyvsidabris ir kopernikas.
- 3B šeima: skandio, itrio ir lantanido serijos (15 elementų) ir aktinidai (15 elementų).
- 4B šeima: titanas, cirkonis, hafnis ir rutherfordis.
- 5B šeima: vanadis, niobis, tantalas ir dubnis.
- 6B šeima: chromas, molibdenas, volframas ir jūrinis borgas.
- 7B šeima: manganas, technecis, renis ir bohris.
- 8B šeima: geležis, rutenis, osmis, hasis, kobaltas, rodis, iridis, meitneriumas, nikelis, paladis, platina, darmstadis.
Nusprendus Tarptautinei grynosios ir taikomosios chemijos sąjungai (IUPAC), grupės pradėtos organizuoti skaičiais nuo 1 iki 18, nors vis dar įprasta šeimas apibūdinti raidėmis ir skaičiais, kaip parodyta aukščiau.
Svarbus skirtumas, kurį sugeneravo nauja IUPAC sistema, yra tai, kad 8B šeima atitinka 8, 9 ir 10 grupes periodinėje lentelėje.
Juodai balta periodinė lentelė
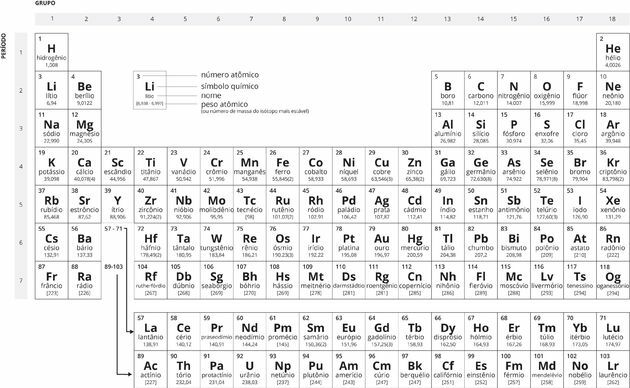
Periodinės lentelės istorija
Pagrindinis lentelės kūrimo tikslas buvo palengvinti elementų klasifikavimą, organizavimą ir grupavimą pagal jų savybes.
Kol nepasiekė dabartinio modelio, daugelis mokslininkų sukūrė lenteles, kurios galėtų parodyti būdą organizuoti cheminius elementus.
Išsamiausią periodinę lentelę sudarė Rusijos chemikas Dmitrijus Mendelejevas (1834-1907), 1869 metais dėl atominė masė elementų.
Mendelejevas išdėstė elementų grupes pagal panašias savybes ir paliko tuščių vietų elementams, kurie, jo manymu, dar bus atrasti.
Periodinę lentelę, kurią mes šiandien žinome, organizavo Henris Moseley, 1913 m., įsakymu atominis skaičius cheminių elementų, pertvarkant Mendelejevo pasiūlytą lentelę.
Williamas Ramsay atrado elementus neoną, argoną, kriptoną ir ksenoną. Šie elementai kartu su heliu ir radonu į periodinę lentelę įtraukė tauriųjų dujų šeimą.
Glennas Seaborgas atrado transuraninius elementus (numeriai nuo 94 iki 102) ir 1944 m. pasiūlė pertvarkyti periodinę lentelę, aktinidų seriją padėdami žemiau lantanidų serijos.
2019 m. Periodinei lentelei sukanka 150 metų ir buvo sukurta Jungtinių Tautų ir UNESCO rezoliucija, kad šie metai taptų Metais Tarptautinė periodinė cheminių elementų lentelė kaip būdas atpažinti vieną įtakingiausių ir svarbiausių kūrinių mokslo.
Periodinės lentelės įdomybės
- Tarptautinė grynosios ir taikomosios chemijos sąjunga Tarptautinė grynosios ir taikomosios chemijos sąjunga - IUPAC) yra nevyriausybinė organizacija (nevyriausybinė organizacija), skirta studijoms ir pažangai Chemija. Visame pasaulyje Organizacija rekomenduoja periodinei lentelei nustatytą standartą.
- Prieš 350 metų pirmasis laboratorijoje išskirtas cheminis elementas buvo fosforas pateikė vokiečių alchemikas Henningas Brandas.
- Plutonio elementą 1940-aisiais atrado amerikiečių chemikas Glennas Seaborgas. Jis atrado visus transuraninius elementus ir 1951 m. Laimėjo Nobelio premiją. 106 elementas jo garbei buvo pavadintas Seaborgium.
- 2016 m. Buvo oficialiai patvirtinti nauji cheminiai lentelės elementai: „Tennessine“ („Ununséptio“), „Nihonium“ („Ununtrio“), „Moscovium“ („Ununpêntio“) ir „Oganesson“ („Ununóctio“).
- Nauji sintetinti cheminiai elementai vadinami itin sunkiais, nes juose yra daug protonai, kuris pasirodo gerokai pranašesnis už gamtoje randamus cheminius elementus.
Periodinės lentelės santrauka
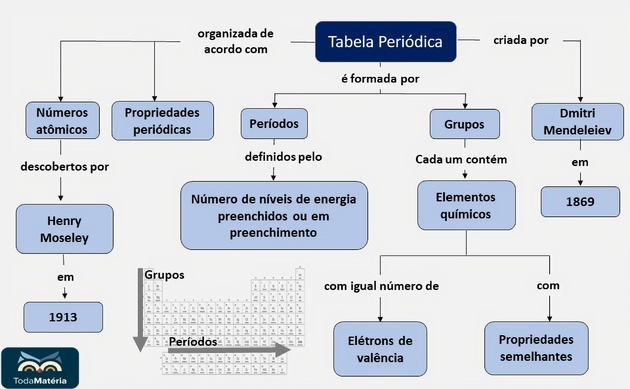
Patikrinkite stojamojo egzamino klausimus komentuodami rezoliuciją Periodinės lentelės pratimai ir neskelbti klausimai Periodinės lentelės organizavimo pratimai.