Rūgštys ir bazės yra dvi tarpusavyje susijusios cheminės grupės. Jie yra dvi labai svarbios medžiagos, kurios yra kasdieniniame gyvenime.
Rūgštis ir bazes tiria neorganinė chemija - šaka, tirianti junginius, kurių nesudaro anglis.
Rūgščių ir bazių sąvokos
Arrenijaus samprata
Viena pirmųjų rūgščių ir bazių sąvokų, kurią XIX amžiaus pabaigoje sukūrė Švedijos chemikas Svante Arrhenius.
Pasak Arrhenijaus, rūgštys yra medžiagos, kurios kenčia vandeniniame tirpale jonizacija, išleidžiant kaip katijonus tik H +.
HCl (aq) → H+ (aq) + Cl- (čia)
Tuo tarpu pagrindai yra kenčiančios medžiagos joninis atsiribojimas, išskirdamas vienintelį anijono tipą OH- (hidroksil) jonus.
NaOH (vandeninis) → Na+ (aq) + OH- (čia)
Tačiau Arrheniuso rūgščių ir bazių koncepcija apsiribojo vandeniu.
Taip pat skaitykite apie: Arrenijaus teorija ir Neutralizavimo reakcija.
Bronstedo-Lowry koncepcija
Bronsted-Lowry koncepcija yra platesnė nei Arrhenius ir buvo pristatyta 1923 m.
Pagal šį naują apibrėžimą rūgštys yra medžiagos, galinčios dovanoti protoną H
+ į kitas medžiagas. Bazės yra medžiagos, galinčios priimti H protoną+ kitų medžiagų.Tai yra rūgštis yra protonų donoras, o bazė - protonų receptorius.
Tai apibūdina a stipri rūgštis kaip visiškai jonizuojantis vandenyje, tai yra, išskiria H jonus+.
Tačiau medžiaga gali būti amfifrotinė, tai yra, gebanti elgtis kaip a rūgštis arba Bronstedo pagrindas. Pažvelkite į vandens pavyzdį (H2O), amfifrotinė medžiaga:
HNO3(aq) + H2O(l) → NE3- (aq) + H3O+(aq) = Bronsted bazė, priėmė protoną
NH3(aq) + H2O(l) → NH4+(aq) + OH-(aq) = Bronstedo rūgštis, paaukotas protonas
Be to, medžiagos elgiasi kaip konjuguotos poros. Visos reakcijos tarp rūgšties ir a bazė iš Bronstedo apima protono perdavimą ir turi dvi konjuguotas rūgščių ir šarmų poras. Žr. Pavyzdį:
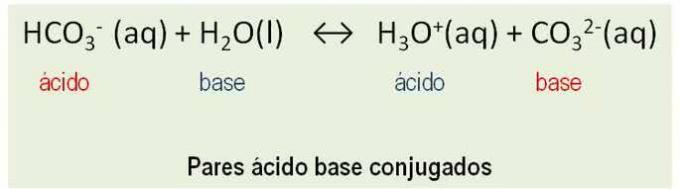
HCO3- ir CO32-; H2O ir H3O+ yra konjuguotos rūgšties bazės poros.
Išmokti daugiau apie:
- Neorganinės funkcijos
- Rūgštinės bazės rodikliai
- Titravimas
Rūgščių nomenklatūra
Norint apibrėžti nomenklatūrą, rūgštys skirstomos į dvi grupes:
- Hidracidai: rūgštys be deguonies;
- Oksirūgštys: rūgštys su deguonimi.
Hidracidai
Nomenklatūra pateikiama taip:
rūgštis + elemento pavadinimas + hidras
Pavyzdžiai:
HCl = druskos rūgštis
HI = vandenilio rūgštis
HF = vandenilio fluorido rūgštis
oksirūgštys
Oksirūgščių nomenklatūroje laikomasi šių taisyklių:
Tu standartinės rūgštys kiekvienos šeimos (periodinės lentelės 14, 15, 16 ir 17 šeimos) vadovaujasi bendrąja taisykle:
rūgštis + elemento pavadinimas + ic
Pavyzdžiai:
HClO3 = chloro rūgštis
H2TIK4 = sieros rūgštis
H2CO3: anglies rūgštis
Kitoms rūgštims, kurios susidaro su tuo pačiu pagrindiniu elementu, mes jas pavadiname pagal deguonies kiekį, laikydamiesi šios taisyklės:
| Deguonies kiekis, palyginti su standartine rūgštimi | Nomenklatūra |
|---|---|
| + 1 deguonis | Rūgštis + elemento pavadinimas + iko |
| - 1 deguonis | Rūgštis + elemento pavadinimas + kaulas |
| - 2 oksigenai | Rūgštis + hipoglikemija + elemento pavadinimas + kaulas |
Pavyzdžiai:
HClO4 (4 deguonies atomai, vienas daugiau nei standartinė rūgštis): perchloro rūgštis;
HClO2 (2 deguonies atomai, vienu mažiau nei standartinė rūgštis): chloro rūgštis;
HClO (1 deguonies atomas, dviem mažiau nei standartinė rūgštis): hipochlorito rūgštis.
Jus taip pat gali sudominti: sieros rūgšties
Bazinė nomenklatūra
Bazinei nomenklatūrai laikomasi bendros taisyklės:
Hidroksidas + katijono pavadinimas
Pavyzdys:
NaOH = Natrio hidroksidas
Tačiau kai tas pats elementas suformuoja katijonus su skirtingais krūviais, jonų krūvio skaičius pridedamas prie vardo pabaigos, romėniškais skaitmenimis.
Arba galite pridėti galūnę -oso prie mažiausiai įkrauto jono ir priesagą -ico prie labiausiai įkrauto jono.
Pavyzdys:
Geležis
Tikėjimas2+ = Fe (OH)2 = Geležies II hidroksidas arba geležies hidroksidas;
Tikėjimas3+ = Fe (OH)3 = Geležies III hidroksidas arba geležies hidroksidas.
Būtinai patikrinkite įstojimo egzamino klausimus šia tema, komentuodami rezoliuciją: Neorganinių funkcijų pratimai.