Anglies monoksidas yra bespalvės, bekvapės, degios ir toksiškos dujos.
Jo molekulinė formulė yra CO. Jis susideda iš anglies ir deguonies molekulės.
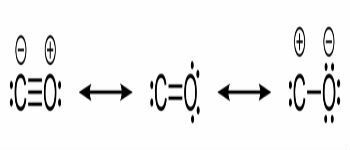
Anglies monoksido ir cheminių jungčių tarp anglies ir deguonies struktūrinės formulės
Jis kyla dviem būdais:
- Natūralūs transliacijos šaltiniai: ugnikalnių, gamtinių dujų ir elektrinių išmetimų aktyvumas.
- žmogaus veikla: rezultatas degimas neišsamus iškastinis kuras. Deginant susidaro tonos CO, tai yra viena iš pagrindinių veiklų, išskiriančių CO į atmosferą.
funkcijos
Anglies monoksidas priklauso oksidai. Jis klasifikuojamas kaip neutralus oksidassusidaro iš metalo ir deguonies. Be to, jis nereaguoja su vandeniu, rūgštimis ir bazėmis.
Jis naudojamas kaip reduktorius, jis pašalina deguonį iš junginio ir gamina anglies dvideginis (CO2). Todėl labai dažnai jis naudojamas apdirbant rūdas, pavyzdžiui, geležį. Taip pat organinių medžiagų, tokių kaip acto rūgštis, plastikai, metanolis, gamyboje.
Reaguodamas su ore esančiu deguonimi, jis gamina anglies dioksidą. Pagal šią cheminę reakciją: 2 CO + O2 → 2 CO2
Paviršiniuose vandenyse didelė anglies monoksido koncentracija tarnauja kaip energijos šaltinis mikroorganizmams.
Anglies monoksidas yra viena iš šiltnamio efektas. Jo koncentracija atmosferoje prisideda prie didesnio šilumos sulaikymo. Todėl jos laikomos teršiančiomis dujomis.
Apsvaigimas
CO pasižymi dideliu afinitetu hemoglobinui. Kadangi jis yra toksiškas, jo įkvėpimas daro poveikį žmonių sveikatai ir netgi gali sukelti mirtį.
Kadangi CO neturi kvapo, jis gali būti neįkvėptas. Todėl kai kuriais atvejais asmuo užtrunka ilgai, kol pastebi apsvaigimą.
Įkvėpus mažai koncentracijos, tai sukelia migreną, lėtą mąstymą, akių dirginimą ir rankinių gebėjimų praradimą. Didelėje koncentracijoje jis gali sukelti traukulius, prarasti sąmonę ir net mirtį nuo uždusimo.
Bet kaip nutinka apsvaigimas?
hemoglobinas jungiasi, žinoma, su O2 ir perneša jį į kūno audinius. Tačiau afinitetas tarp CO ir hemoglobino yra daug didesnis, maždaug 250 kartų didesnis nei su O2.
Esant CO, hemoglobinas prie jo prisijungia, neleisdamas deguoniui pernešti į ląsteles. CO derinys su hemoglobinu sukelia karboksihemoglobiną.
Pagrindinės apsinuodijimo CO priežastys atsiranda šiose situacijose:
- Automobilių varikliai, dirbantys patalpose;
- Nudegimas gamtinių dujų neefektyviuose šildytuvuose;
- Dujos iš virtuvės ar medienos krosnies, blogai vėdinamose vietose.
Šaltuose klimato kraštuose namai būna ilgiau uždaryti ir naudoja šildymo sistemas. Siekiant išvengti dujų avarijų, vis dažniau naudojami CO detektoriai.
Sužinokite daugiau, taip pat skaitykite:
- anglies ciklas
- Anglis
- Iškastinis kuras
- Deguonis