At organinės eliminacijos reakcijos yra tie, kuriuose molekulės atomai ar atomų grupės yra pašalinami arba pašalinami iš jos, sukuriant naują organinį junginį, be neorganinio junginio, kuris susidaro iš buvusios dalies ištrintas.
Viena eliminacijos reakcijos rūšis yra dehidracija, kurioje prarasta molekulė yra vanduo. Alkoholių (junginių, turinčių OH grupę prie prisotintos anglies atviroje grandinėje) dehidracija gali vykti dviem būdais: intramolekulinis ir tarpmolekulinis.
„Intra“ reiškia „viduje“, todėl intramolekulinė alkoholių dehidracija įvyksta, kai vandens molekulė išeina iš pačios alkoholio molekulės „vidaus“. Tokiu atveju susidaręs organinis produktas bus alkenas.
Ši reakcija vyksta tik esant katalizatoriui, kuris veikia kaip sausiklis, ir dažniausiai tai yra koncentruota sieros rūgštis (H2TIK4), o temperatūra turėtų būti apie 170ºC.
Pavyzdys:
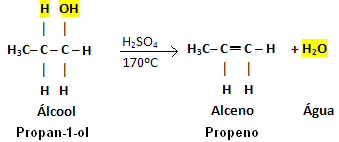
Atkreipkite dėmesį, kad OH grupė išėjo, o vandenilis paliko kaimyninę anglį, todėl atsirado vanduo. Be to, buvo sukurtas dvigubas ryšys, dėl kurio atsirado alkenas.
Dehidracijos patiriama mažėjančia tvarka:
Tretiniai alkoholiai> Antriniai alkoholiai> Pirminiai alkoholiai
Bet ką daryti, kai OH grupė patenka į anglies grandinės vidurį? Vandenilio atomas, iš kurio išsiskirs kaimyninis anglies atomas ir sudarys vandens molekulę?
Nesustokite dabar... Po reklamos yra daugiau;)
Pavyzdžiui, kitas yra 2-metilpentan-3-olis. Atkreipkite dėmesį, kad vienas kaimyninis anglies atomas yra tretinis (paryškintas raudonai), o kitas yra antrinis (pažymėtas mėlyna spalva):
H OH H
│ │ │
H3C─ Ç ─ Ç ─ Ç CH3
│ │ │
H H CH3
Vandenilį, sujungtą su tretiniu anglies atomu, bus lengviau palikti, nes jo elektronegatyvus yra lygus δ+1Taigi, kuo mažiau neigiamas anglies pobūdis, tuo silpnesnis ryšys tarp jų ir lengviau bus nutraukti jų ryšį.
Tokiais atvejais susidaro visi įmanomi junginiai, tačiau persvara bus pateikiama tokia tvarka: Tretiniai alkoholiai> Antriniai alkoholiai> Pirminiai alkoholiai.
Taigi mes turime:
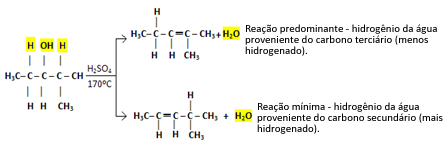
Šio tipo reakcijos paklūsta Saytzefo taisyklė, kuris tai sako bus didesnė tendencija, kad vandenilis liks mažiau hidrintas anglies. Ši taisyklė yra visiškai priešinga Markovnikovo taisyklė naudojamas pridėjimo reakcijoms.
Norėdami papildyti savo žinias šia tema, taip pat perskaitykite tekstą "Tarpmolekulinė alkoholių dehidracija”.
Jennifer Fogaça
Baigė chemiją
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Tarpmolekulinė alkoholių dehidracija“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm. Žiūrėta 2021 m. Birželio 28 d.

