Kai kuriems junginiams, norint pasiekti stabilumą, valentiniame apvalkale nereikia turėti aštuonių elektronų, todėl jie laikomi aštuonetės taisyklės išimtimis. Sužinokite dabar, kodėl kai kurie elementai neišvengia pareigos paskutiniame apvalkale turėti elektronų oktetą.
Berilis (Būti)
Tai yra aštuonetės taisyklės išimtis, nes ji gali sudaryti junginius su dviem viengubais ryšiais, todėl stabilizuojasi tik valentiniame apvalkale esantiems keturiems elektronams. 
Kadangi vandeniliui (H) užmegzti ryšį reikia atsisakyti dviejų elektronų (H - Na - H), berilio (Be) atomas dalijasi savo elektronais ir pasiekia stabilumą.
Aliuminis (Al)
Tai yra aštuoneto taisyklės išimtis, nes ji pasiekia stabilumą su šešiais elektronais valentiniame apvalkale. Aliuminio atomas linkęs dovanoti savo elektronus, todėl gali sudaryti tris viengubus ryšius su kitais atomais: 
Šiuo atveju aliuminis (Al) suformavo tris jungtis su trim fluoro (F) atomais.
Boras (B)
Jis suformuoja molekulines medžiagas su trimis viengubais ryšiais.
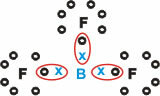
Atkreipkite dėmesį, kad boras (B) yra linkęs paaukoti savo elektronus fluoro (F) atomams, kurie laikosi aštuoneto taisyklės, o valentiniame apvalkale reikalingi aštuoni elektronai. Kai boras atsisako savo elektronų, fluoras stabilizuojasi su susidariusiu oktetu.
Autorius Líria Alves
Baigė chemiją
Brazilijos mokyklos komanda
Nesustokite dabar... Po reklamos yra daugiau;)
Žiūrėti daugiau!
Aštuoneto teorija
Bendroji chemija - Chemija - Brazilijos mokykla
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
SOUZA, Líria Alves de. „Aštuonetės taisyklės išimtys“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm. Žiūrėta 2021 m. Birželio 27 d.

