At degimo reakcijos jų yra daugelyje mūsų kasdienio gyvenimo aspektų. Pavyzdžiui, pagrindiniai energijos gamybos šaltiniai susidaro deginant ar deginant tam tikrus degalus, pavyzdžiui, etanolį, benziną, anglį. Be to, energija, kurios mums reikia norint išgyventi ir dirbti, yra degimo reakcijų, vykstančių mūsų ląstelėse, kai „deginame“ valgomą maistą, rezultatas.
Bet ko reikia, kad susidarytų degimo reakcija?
Reikia trijų dalykų:
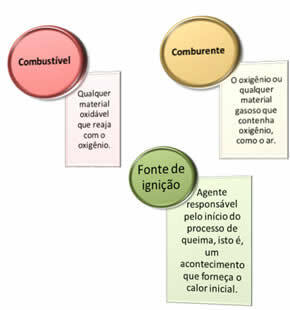
Šie trys veiksniai sudaro ugnies trikampis, nes prasidėjus degimo reakcijai, išsiskyrusi energija palaiko reakciją ir leidžia jai tęstis tol, kol dings kuras, oksidatorius ar šiluma (išsiskyrusi energija). Tai reiškia, kad bus a Grandininė reakcija.
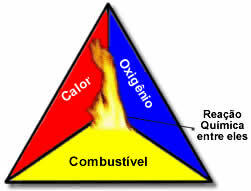
Pavyzdžiui, jei kas nors įmeta uždegtą cigaretę į mišką, kils gaisras (degimo reakcija). Šiuo atveju krūmas tai kuras, O deguonies, esančio ore atmosferos yra oksidatorius tai cigaretė dega buvo uždegimo šaltinis. Šis deginimas tęsis tol, kol bus pašalintas vienas iš trijų veiksnių. Jei ugniagesiai gesins vandenį, šiluma bus pašalinta. Bet net jei nieko nedaroma, kad šis degimas būtų sustabdytas, jis tam tikru momentu baigsis, tai yra, kai baigsis kuras (miškas).
Kaip jau minėta, šiose reakcijose išsiskiria šiluma, taigi degimas yra egzoterminė reakcija. Tačiau tokio tipo reakcijos yra nepilnas degimas. Norėdami suprasti, kodėl, pamatykite skirtumą tarp visiško ir nebaigto degimo:
Nesustokite dabar... Po reklamos yra daugiau;)
Visiškas degimas:
Analizuodami organinius junginius kaip kurą, turime:
| visiškas degimas jis įvyks, kai anglies grandinė nutrūks ir visi anglies atomai anglies grandinėje bus visiškai oksiduoti. |
| Tu suformuoti produktai angliavandeniliais bus CO2 (anglies dioksidas) ir H2O (Vanduo). |
Stebėkite visišką izoktano, kuris yra vienas iš benzino komponentų, degimą.
Ç8H18 g) +25/2 O2 g) → 8 CO2 g) + 9 val2O(1)
Nebaigtas degimas
| Šiuo atveju nepakanka oksidatoriaus, tai yra pakankamai deguonies, kad būtų sudeginti visi degalai. |
| Taigi susidarę produktai yra CO (anglies monoksidas) ir H2O. |
Stebėkite tą patį izoktano degimą, tačiau dabar jis nevisiškai:
Ç8H18 g) + 17/2 O2g) → 8 CO g) + 9 val2O(1)
Miškų deginimas yra pavyzdys, nes susidaro CO ir tam tikros medžiagos, tokios kaip suodžiai (C), taip pat pelenai ir kiti paprasti ir sudėtingi organiniai junginiai. Azoto oksidas, ozonas ir aldehidai taip pat gali susidaryti dėl antrinių reakcijų, nes ore yra kitų komponentų.
Ç8H18 g) + 9/2 O2 g) → 8C g) + 9 val2O(1)
Jennifer Fogaça
Baigė chemiją
Brazilijos mokyklos komanda
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Visiškas ir nebaigtas degimas“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Žiūrėta 2021 m. Birželio 27 d.



