Tekstas Titravimas parodė, kaip atliekama ši tūrio analizės technika, kurios pagrindinis tikslas yra nustatyti tirpalo koncentraciją reaguojant su kitu žinomos koncentracijos tirpalu.
Dabar pamatysime, kaip panaudoti titravimo metu gautus duomenis, norint pasiekti norimą koncentraciją, kuri gali būti rūgštis arba bazė tirpale. Norėdami tai padaryti, iš esmės yra trys žingsniai:
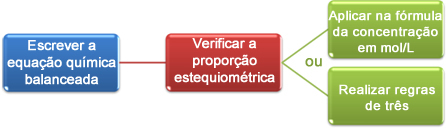
Pažvelkime į pavyzdį:
Tarkime, chemikas turėjo acto rūgšties (acto (CH3COOH(čia))) ir norėjo sužinoti jo koncentraciją mol / l. Tada jis įdėjo 20,0 ml acto (titruojamo) į Erlenmeyerio kolbą ir pridėjo fenolftaleino indikatorių. Tada jis užpildė 100 ml biuretą natrio hidroksidu (NaOH), kurio koncentracija (titrantas) buvo lygi 1,0 mol / l. Galiausiai chemikas atliko titravimą ir pastebėjo, kad spalvos pasikeitimas (posūkio taškas - kai jis sustabdė titravimą) įvyko, kai buvo suvartota 24 ml NaOH.

Remdamasis šiuo eksperimentu, jis gavo šiuos duomenis:
MCH3COOH= ?
VCH3COOH = 20 ml = 0,02 l
MNaOH = 24 ml = 0,024 l
VNaOH = 1,0 mol / l
Kur M = koncentracija mol / l ir V = tūris L.
Norėdami sužinoti acto rūgšties koncentraciją, pirmiausia turime žinoti, kaip užrašyti cheminę lygtį, kuri atspindi įvykusią tinkamai subalansuotą neutralizavimo reakciją. Šiuo atveju reakcija yra tokia:
1 CH3COOH(čia) + 1 NaOH(čia) → 1 NaC2H3O2 (aq) + 1 valanda2O(ℓ)
Ši dalis yra svarbi norint pamatyti stechiometrinį santykį, kuriuo reaguoja reagentai. Atkreipkite dėmesį, kad santykis yra 1: 1, tai yra, kiekvienam acto rūgšties moliui reikia 1 molio natrio hidroksido.
Dabar skaičiavimus galime atlikti dviem būdais:
(1) Pagal formulę: M1. V1 = M2. V2
Kadangi stechiometrinis santykis yra 1: 1, turime: neCH3COOH = nNaOH .
Nesustokite dabar... Po reklamos yra daugiau;)
Esamas M = n / V → n = M. V. Taigi mes pasiekiame aukščiau pateiktą sąrašą, kurį šiuo atveju galima parašyti taip: MCH3COOH. CH3COOH = MNaOH. VNaOH
Taigi, tiesiog pakeiskite šios formulės reikšmes:
MCH3COOH. V CH3COOH = MNaOH. VNaOH
MCH3COOH. 0,02 l = 1,0 mol / l. 0,024 l
MCH3COOH = 0,024 mol
0,02 l
MCH3COOH = 1,2 mol / l
Todėl pradinė acto rūgšties tirpalo, mūsų pavadinimo, koncentracija buvo 1,2 mol / l.
Svarbi pastaba: Jei stechiometrinis santykis nebūtų 1: 1, pakaktų medžiagų koncentraciją mol / L (M) padauginti iš jų atitinkamų koeficientų. Pavyzdžiui, jei santykis būtų 1: 2, turėtume:
M1. V1 = 2. M2. V2
Bet čia yra dar vienas būdas atlikti šiuos skaičiavimus:
(2) Pagal trijų taisykles:
1 CH3COOH(čia) + 1 NaOH(čia) → 1 CH3COONa(čia) + 1 valanda2O(ℓ)
1 mol 1 mol 1 mol 1 mol
1. 60 g 1. 40 g 1. 82 g 1. 18 g
Šios masės yra apskaičiuotos kiekvienos medžiagos molekulinės masės.
* Žinodamas, kad panaudotas 1,0 mol / l NaOH tirpalo tūris(čia) buvo 24 ml, pirmiausia galime sužinoti reagavusios NaOH medžiagos kiekį (mol):
1 mol NaOH → 1,0 l
1 mol NaOH 1000 ml
x 24 ml
x = 0,024 mol NaOH
* Kadangi santykis yra 1: 1, acto rūgšties medžiagos (mol) kiekis turėtų būti toks pat kaip NaOH: 0,024 mol.
Stebėjimas: Jei stechiometrinis santykis būtų kitoks, šioje dalyje į tai atsižvelgtume. Pavyzdžiui, jei jis būtų 1: 3, o vienos chemiškai reaktyvios rūšies medžiagos kiekis būtų lygus 0,024 mol, tai kitos medžiagos kiekis būtų trigubas: 0,072.
* Dabar mes apskaičiuojame:
20 ml acto 0,024 mol acto rūgšties
1000 ml acto ir
y = 1,2 mol
Tai yra, yra 1,2 mol / l, tai yra ta pati vertė, kurią gavome taikant ankstesnį metodą.
Jennifer Fogaça
Baigė chemiją