Tu aldehidai ir ketonai jie yra labai panašios organinės funkcijos. Abiejų struktūroje yra funkcinė karbonilo grupė (C = O), turint vienintelį skirtumą aldehidai, jis visada pasirodo anglies grandinės gale, tai yra vienas iš karbonilo anglies ligandų yra vandenilis; ketonai turi karbonilą tarp dviejų kitų anglies atomų.
Aldehidų funkcinė grupė:Funkcinė ketonų grupė:
O O
║ ║
C C ─ H C C - C
Dėl šios priežasties yra funkcinio izomerizmo atvejų tarp aldehidų ir ketonų. Pavyzdžiui, žemiau pateikiame du funkcinius izomerus, kurių molekulinė formulė yra ta pati (C3H6O), bet vienas yra aldehidas (propanalas), kitas - ketonas (propanonas). Sužinokite, kaip tai visiškai pakeičia jų savybes ir programas:
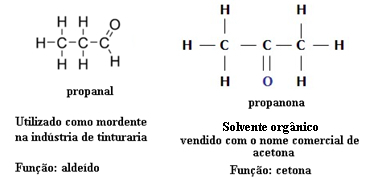
Funkcijos izomerijos tarp aldehido ir ketono pavyzdys
Įsivaizduokite, kad esate laboratorijoje ir rasite buteliuką su bespalviu skysčiu, kurio molekulinė formulė yra tik C3H6O. Ką darytumėte, kad sužinotumėte, ar tai ketonas, ar aldehidas?
Norėdami išspręsti tokias problemas, yra aldehidų ir ketonų diferenciacijos metodų, pagrįstų šių junginių reakcija su silpnais oksidatoriais
. Kaip parodyta žemiau, susidūrę su silpnais oksidatoriais, aldehidai reaguoja oksiduodamiesi, o ketonai nereaguoja. Mes taip sakomealdehidai veikia kaip reduktoriai, bet ketonai - ne, jie reaguoja tik kaip reduktoriai, besiliečiantys su energetiniais oksidatoriais.Aldehidai + silpni oksidatoriai → karboksirūgštis
O O
║ ║
C ─ C ─ H + [O] → C ─ C ─ OH
Ketonai + silpni oksidatoriai → Nereaguoti
O
║
C ─ C ─ C + [O] → Reakcija nevyksta
Remiantis tuo, pakanka įvykdyti šią reakciją ir pamatyti, ar junginys nereaguoja. Jei jis reaguoja, žinome, kad tai aldehidas; jei jis nereaguoja, tai yra ketonas.
Be to, produktai, susidarantys šiose aldehido oksidacijos reakcijose, yra gana matomi, o spalvos pokyčiai įvyksta, kaip bus parodyta vėliau.
Yra trys pagrindiniai aldehidų ir ketonų diferenciacijos metodai:
1- „Tollens“ reaktyvus: Šis reagentas yra a sidabro nitrato amoniako tirpalas, ty jame yra sidabro nitrato (AgNO3) ir amonio hidroksido perteklius (NH4OI):
AgNO3 + 3 NH4OH → Ag (NH3)OI + NH4PRIE3 + 2 H2O
„Tollens Reactive“ (pavadintas vokiečių chemiko Bernhardo Tollenso (1841–1918) vardu)
Kaip paaiškinta tekste Sidabrinio veidrodžio gamyba, kai aldehidas kontaktuoja su reaktyviu „Tollens“, jis oksiduojamas iki atitinkamos karboksirūgšties, o sidabro jonai redukuojami iki Ag0 (metalinis sidabras). Pavyzdžiui, jei ši reakcija atliekama mėgintuvėlyje, šis metalinis sidabras nusėda ant vamzdelio sienelių ir susidaro plėvelė, vadinama sidabrinis veidrodis. Šis pastebėtas rezultatas yra labai gražus ir naudojamas pramoninių veidrodžių gamybos procese.
Vykstanti reakcija gali būti pavaizduota taip:
O O
║ ║
R - C - H + H2O → R ─ C ─ OH + 2e- + 2 H+
2 m+ + 2e- → 2 Ag0
2 NH3 + 2 H+ → 2 NH4+
O O
║║
R C ─ H + 2 m+ + 2 NH3 + H2O → R C - OH + 2 m0 + 2 NH4+
aldehidas Tollensas yra reaktyvuskarboksirūgštis metalinis sidabras (sidabrinis veidrodis)
Kita vertus, jei ketoną pradėsime reaguoti su Tollens reaktyviuoju, metalinis sidabras nesusidarys, nes ketonai negali sumažinti Ag jonų.+.
2- Fehling reaktyvus: Šis reaktyvus yra mėlynas vario sulfato II (CuSO4) bazinėje terpėje, nes jis sumaišomas su kitu natrio hidroksido (NaOH) ir natrio ir kalio tartrato (NaOOC-CHOH-CHOH-COOK) susidariusiu tirpalu. Kad stabilizuotųsi ir būtų išvengta nuosėdų, į vario II sulfato tirpalą įpilama tartrato.
CUSO4 + 2 NaOH → Na2TIK4 + Ku (OH)2
„Fehling Reactive“ (pavadintas vokiečių chemiko Hermano von Fehlingo (1812–1885) vardu)
Susilietęs su reaktyviuoju Fehlingo aldehidu oksiduodamasis susidaro karboksirūgštis, o vario jonai (Cu)2+), esančios viduryje, redukuojamos, susidaro rausvai rudos nuosėdos (labiau panašios į plytas), kurios yra vario oksidas. Kita vertus, ketonai nereaguoja, nes jie negali sumažinti Cu jonų2+.
O O
║ ║
R - C - H + 2 Cu (OH)2 → R ─ C ─ OH + Asilas2O + 2 H2O
aldehidas rausvai rudos nuosėdos
3- Benedikto reaktyvumas: Šis reaktyvus susidaro ir iš vario II sulfato tirpalo (Cu (OH)2) bazinėje terpėje, tačiau jis sumaišomas su natrio citratu.
Kaip ir Fehlingo reagento atveju, reakcijos tarp aldehido ir Benedikto reagento atveju taip pat yra vario jonų (Cu2+) terpėje yra redukuotų ir susidaro raudonasis vario oksidas.
Šis reagentas plačiai naudojamas atliekant tyrimus siekiant nustatyti gliukozės kiekį ir kiekį šlapime. Gliukozės struktūra turi aldehido grupę, todėl šioms reakcijoms ji reaguoja su juostose esančiu Benedikto reagentu. Tiesiog palyginkite juostelės spalvą su gaminio pakuotės skalės spalva.

Benedikto reagentas naudojamas gliukozės kiekiui šlapime nustatyti.
Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm

