에너지내부의 의 합계입니다 운동 에너지 그리고 신체의 구성 원자 및 분자의 움직임과 관련된 잠재력. 내부 에너지는 또한 온도 몸의. 줄 (SI)로 측정 된 스칼라 수량이며 다음과 같은 변수의 함수로 결정됩니다. 압력 (피), 음량 (V) 및 온도 시스템의 열역학 (T), 켈빈 (K).
신체의 온도가 높을수록 내부 에너지가 커지므로 어떤 일을 할 수있는 능력이 커집니다. 또한, 예를 들어 단일 원자 가스의 내부 에너지는 운동 에너지 가스의 모든 원자의. 이원자 가스와 같은 분자 가스를 다룰 때는 분자 상호 작용을 고려해야합니다. 이 내부 에너지는 분자의 운동 에너지와 그 사이에 존재하는 위치 에너지의 합에 의해 결정됩니다. 그들.
지금 멈추지 마세요... 광고 후 더 있습니다;)
이상적인 단일 원자 가스의 내부 에너지
이상적인 단일 원자 가스의 원자간에 상호 작용이 없기 때문에 내부 에너지는 몰수 (n)와 가스 온도 (T)의 두 가지 변수에만 의존합니다. 손목 시계:
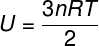
유 – 내부 에너지
아니 – 두더지 수
아르 자형 – 완벽한 기체의 보편적 상수
티 – 온도
위의 방정식에서 아르 자형 계수는 0.082 atm입니다. L / 몰. K 또는 8.31 J / mol. K (SI). 또한 압력 및 부피와 같은 다른 양으로 위의 방정식을 작성할 수 있습니다. 이를 위해 우리는 Clapeyron의 방정식, 이상 기체에 사용됩니다.
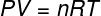
위의 방정식을 이전 방정식으로 대체하면 내부 에너지 계산을 위해 다음과 같은 표현식이 있습니다.
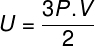
보기또한:완벽한 기체는 무엇입니까?
위의 방정식을 고려하면 이상적인 단일 원자 가스 원자의 운동 에너지와 온도 사이의 관계를 결정할 수 있습니다. 이를 위해 우리는 이러한 유형의 가스의 운동 에너지가 전혀동력학. 손목 시계:
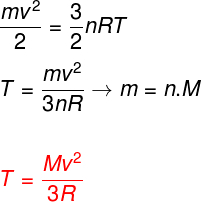
미디엄 - 파스타
아니 – 몰수
미디엄 -몰 질량
많은 상황에서 가스의 내부 에너지 (ΔU) 변화를 계산하는 방법을 아는 것은 흥미 롭습니다.이 양은 가스가 받았다 또는 주다 에너지. 가스 내부 에너지의 변화가 양수 (ΔU> 0)이면 가스에 에너지가 공급됩니다. 그렇지 않으면 (ΔU <0) 가스가 에너지의 일부를 포기하게됩니다.
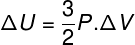
가스 부피 변화 측면에서 내부 에너지 변화.
이원자 가스의 내부 에너지
이상적인 이원자 가스의 경우 내부 에너지는 약간 다른 방정식으로 제공됩니다.
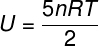
열역학적 변환 및 순환의 내부 에너지
에 따르면 열역학 제 1 법칙, 이상 기체의 내부 에너지는 열역학적 변환, 주변과 시스템 사이에서 교환되는 열량과 시스템에서 수행하는 작업에 따라 다릅니다.
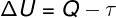
큐 – 열
τ -일
다음으로, 이 법칙이 특정한 열역학적 변환에 대해 취하는 형식을 살펴 보겠습니다.
보기또한:열 기계의 역사
→ 내부 에너지: 등온 변환
에서 등온 변환, 온도 변화가 없으므로 내부 에너지가 일정하게 유지됩니다.
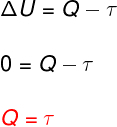
이 경우 시스템과 교환되는 전체 열량이 작업으로 전환되고 그 반대의 경우도 마찬가지입니다.
→ 내부 에너지: isovolumetric 변환
에서 isovolumetric 변환, 시스템이 견고하고 팽창 할 수없는 용기에 갇혀 있기 때문에 작업을 수행 할 수 없습니다. 이 경우 시스템과 교환되는 전체 열량은 내부 에너지를 직접 변경합니다.
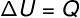
→ 내부 에너지: 등압 변환
이러한 유형의 변환에서 시스템은 일정한 압력따라서 그 또는 그에 대한 작업을 분석적으로 계산할 수 있습니다.
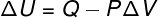
→ 내부 에너지: 단열 변환
에서 단열 변환, 시스템과 주변 환경간에 열 교환이 없기 때문에 내부 에너지의 변화는 시스템에서 수행하는 작업에만 의존합니다.
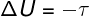
순환 과정의 내부 에너지
모든 순환 과정에서 압력, 부피 및 온도 변수 (P, V, T)로 표현되는 시스템의 열역학적 상태는 다음과 같습니다. 그러나 원래 상태 (P, V, T)로 돌아 가게되므로 이러한 유형의 프로세스에서 내부 에너지의 변화는 항상 null입니다 (ΔU = 0).
보기또한:순환 변환
상태 A와 B 사이의 세 가지 뚜렷한 열역학적 변환을 보여주는 아래 그래프를보십시오.
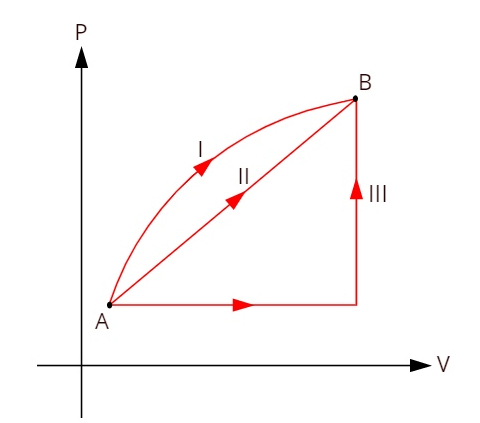
세 가지 변환 (I, II 및 III)이 상태 A를 떠나 상태 B로 이동함에 따라 내부 에너지 변동은 모두 동일해야합니다.
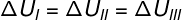
내부 에너지 운동
1) 몰 질량이 24g / mol 인 2 몰의 이상적인 이원자 가스는 부피가 10 인 밀폐 된 단단한 용기 내부에서 500K의 온도에서 발견됩니다.-3 m³. 결정:
a)이 기체의 내부 에너지 모듈러스 (줄 단위).
b) 가스가 용기 벽에 가하는 압력.
해결:
그만큼) 이상적인 이원자 기체이기 때문에 아래 공식을 사용하여 내부 에너지를 계산합니다.
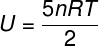
연습 보고서에 제공된 데이터를 사용하여 다음 계산을 해결해야합니다.
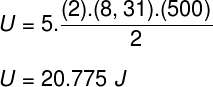
비) 용기의 부피를 알면 가스가 가하는 압력을 결정할 수 있습니다. 10-3 m³. 이를 위해 다음 공식을 사용합니다.
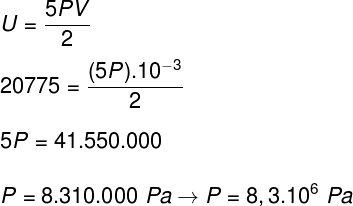
나. Rafael Helerbrock