산 물질은 수성 매체에서 이온화 그리고 좋다 지휘자 힘. 물질의 산도는 수소 이온 전위를 측정하는 기술을 통해 측정 할 수 있습니다 (pH). 일부 pH 분석 방법은 용액의 pH 값을 색상으로 반영하는 리트머스 또는 페놀프탈레인과 같은 지표를 사용합니다.
산은 다음과 같이 특성화 될 수 있습니다.
분자에 산소의 존재 여부에 따라;
강압적으로;
이온화 가능한 수소에 의해;
변동성에 의해.
읽기 :산과 염기의 비교-차이점과 특성
산의 특성
그들은 수성 매체에서 이온화되어 H 양이온을 방출합니다.+.
그들은 방출로 인해 전기 전도체입니다. 이온 수성 매체에서.
기본 환경과 접촉하면 중화 반응,이 반응의 산물로 소금과 물을 형성합니다.
그들은 리트머스 또는 페놀프탈레인과 같은 지표 물질의 존재하에 용액의 색을 변경합니다.
다른 감귤류 중에서도 레몬, 오렌지의 신맛은 이러한 식품에 존재하는 산 때문입니다.
지금 멈추지 마세요... 광고 후 더 있습니다 ;)
수소 전위 (pH)
수소 이온 전위 (pH)는 다음을 표현하는 계산입니다. 이온 농도 수소 어느 정도 해결책. pH를 결정하고 배지를 분석하기 위해 다음 사항이 고려됩니다.
Ostwald의 희석 법칙 (희석할수록 용액에 더 많은 이온이 형성됨)
물자가 이온화 (Kw): H 분자의 자연 분해2H 이온의 O+ 그리고 오-;
25 ° C 증류수에는자가 이온화 Kw = 10-14 동일한 농도의 H 이온+ 그리고 오-즉, 중립 매체입니다.
H 농도를 포함한 pH 계산 용+, 사용하다: pH = -log [H+].
알고:
pH> 7 → 염기성 용액
pH <7 → 산성 용액
pH = 7 또는 pH = pOH → 중성 용액
너무 참조: 산 공식은 어떤가요?

산의 분류
그만큼 산 분류 네 가지 기준을 고려하여 수행 할 수 있습니다.
이온화 정도 (α) 또는 산 강도
α = 이온화 된 분자의 수
용해 된 분자의 수
강산 : α ≥ 50%.
예: á산 황의 (H2뿐4) → α = 61%.반강 또는 중간 산 : 5% < α < 50%.
예: 인산 (H3먼지4) → α = 27%.약산: α ≤ 5%.
예: 붕산 (H3악3) → α = 0,075%.
→ 이온화 가능한 수소의 수
일산: H 양이온 방출+.
예: á산 염산 (HCL);
이산: 두 개의 H 양이온 방출+.
예: 황화수소 (H2에스).삼산: 3 개의 H 양이온 방출+.
예: 붕산 (H3악3).테트라 시드: 4 개의 H 양이온 방출+.
예: 피로 인산 (H4피2영형7).
주의! 수소산의 경우 분자의 모든 수소는 이온화 가능합니다. 그러나 산소산의 경우 산소 원자에 결합 된 수소 만 이온화 할 수 있습니다. 예를 들면 차 아인산 (H3먼지2), 이는 구성에 3 개의 수소가 있음에도 불구하고 결합 된 수소 만 방출하기 때문에 일산입니다. 산소.
→ 산소의 존재
산소산: 구조에 산소가 있습니다.
예: 차아 염소산 (HO Cl).
히드라 산: 구조에 산소가 없습니다.
예: 불산 (HF).
→ 변동성
결정된: 비점(발) > 100 ° C, 천천히 기체 상태로 변합니다.
예: 황산 (H2뿐4) → PE = 340 ° C.휘발성 물질: 끓는점 <100 ° C, 가스 상태로 빠르고 쉽게 변합니다.
예: 황화수소 (H2S) → PE = -59.6 ° C.
산 명명법
→ 히드라 산
산 + 음이온 이름 + hydric
모든 산에 대해 "산"이라는 용어는 분자를 특성화하는 명명법 앞에 사용됩니다. hydracids에서 요소 이름의 접미사 "eto"는 "hydric"으로 대체됩니다.
예:
HCl → 산 염소하이드 릭
HBr → 산 브롬하이드 릭
HF → 산 플루오르하이드 릭
→ 산소산
산소산의 명명법은 다음에 따라 다릅니다. 산화수 (NOX) 중심 요소의. 아래 표를 참조하십시오.
중심 원소의 NOX |
산 명명법 |
||
접두사- |
-중첩- |
-접미사 |
|
+1 및 +2 |
하마 |
-음이온 이름- |
-oso |
+3 및 +4 |
-- |
음이온 이름 |
-oso |
+5 및 +6 |
-- |
음이온 이름 |
-ic |
+7 |
당 |
-음이온 이름- |
-ic |
예:
HClO → 수소 (H)에는 일반적으로 NOX +1이 있고 산소 (O)에는 NOX -2가 있습니다. 차아 염소산.
HNO2 → 아질산
HClO4 →á산과염 소
→ 규칙에 대한 예외
H2CO3 → 탄산, NOX 규칙에 따라 탄소 질이 아닙니다.
H3악3 → á산 붕소, 지루하지 않습니다.
일상 생활의 산
비료 및 의약품 : 인산 (H3먼지4) 비료 제조 및 의약품으로 널리 사용됩니다. 제약 분야에서 사용되는 여러 산 중 하나입니다.
감귤류 : 아스코르브 산 (C6H8영형6), 또한 ~으로 알려진 비타민 C.
식초: 구성에 있음 아세트산 (CH3COOH).
- 탄산수 및 청량 음료 : 탄산 (H2CO3), 제품에 상쾌한 느낌을줍니다.
또한 액세스:청량 음료에서 산의 역할

풀린 연습
질문 1 - (Enem) 적 양배추에서 추출한 주스는 다양한 용액의 산성 특성 (pH 0 ~ 7) 또는 염기성 (pH 7 ~ 14)의 지표로 사용할 수 있습니다. 약간의 배추 즙과 용액을 섞으면 아래 척도에 따라 산성 또는 염기성 특성에 따라 혼합물이 다른 색을 나타 내기 시작합니다.
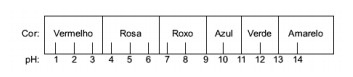
이 표시기로 일부 솔루션을 테스트하여 다음과 같은 결과를 얻었습니다.
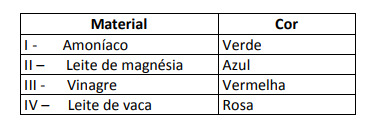
이 결과에 따르면 솔루션 I, II, III 및 IV는 각각 다음과 같은 특성을 갖습니다.
A) 산성 / 염기성 / 염기성 / 산성.
B) 산 / 염기성 / 산 / 염기성.
C) 염기성 / 산성 / 염기성 / 산성.
D) 산 / 산 / 염기성 / 염기성.
E) 염기성 / 염기성 / 산성 / 산성.
해결
대안 E. 물질이 산성, 염기성 또는 중성 특성을 가지고 있는지 여부를 결정하기 위해 주어진 척도의 데이터와 관련하여 테스트에서 얻은 색상의 분석이 수행됩니다. pH = 7 인 용액이 중성이고 pH> 7이 염기성이며 pH가 7 미만인 용액이 산성임을 알면 암모니아와 마그네시아 우유는 기본 물질이고 식초와 우유는 산.
질문 2 - (PUC-Camp) 산이라는 물질에 대해 한 학생은 다음과 같은 특성을 지적했습니다.
나는-부식 력이 있습니다.
II-염기를 중화시킬 수 있습니다.
III-두 가지 화학 원소로 구성됩니다.
IV-전류를 전도하는 수용액을 형성합니다.
그는 실수를 저질렀다.
A) I 및 II
B) I 및 III
C) I 및 IV
D) II 및 III
E) III 및 IV
해결
대안 B. 모든 산이 부식성이있는 것은 아니며 가장 강한 산만 부식성이 있으며 산은 두 개 이상의 원자로 구성 될 수 있습니다.
작성자: Laysa Bernardes
화학 교사
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
ARAúJO, Laysa Bernardes Marques de. "산"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/acidos.htm. 2021 년 6 월 27 일 액세스.


