텍스트에서 "화성 전기 분해”,이 과정은 전류가 녹은 물질 (액체 상태)에 전류가 흐르면 발생한다고 설명했습니다. 이런 식으로 양이온은 전자를 받고 음이온은 전자를 제공하므로 둘 다 0과 같은 전하와 에너지를 갖습니다. 축적.
화성 전기 분해가 어떻게 발생하는지 더 잘 이해하기 위해 이러한 유형의 공정 중 가장 중요한 예 중 하나 인 염화나트륨 또는 식염 (NaCl)의 전기 분해를 고려해 보겠습니다.
염화나트륨은 아래 반응에 따라 나트륨 (Na)에서 염소 (Cl)로 전자를 전달하여 자연적으로 형성됩니다.
2Na (s) + 1Cl2(g) → 2NaCl (s)

이 과정은 자발적이지만이 반응의 역 과정은 자발적인 것이 아닙니다. 즉, 염소 가스 (Cl2(g) – 아래 그림) 및 금속 나트륨 (Na (s))은 자연에서 발생하지 않습니다. 이런 일이 일어나기를 원한다면 프로세스를 시작해야합니다.
이것은 화성 전기 분해에 의해 수행 될 수 있습니다. 소금은 녹는 점 인 800.4 ° C 이상의 온도로 가열됩니다. 이런 식으로 합쳐져 고체에서 액체로 전달됩니다. 이 물리적 상태에서 너의 Na 이온+ 및 Cl- 무료.
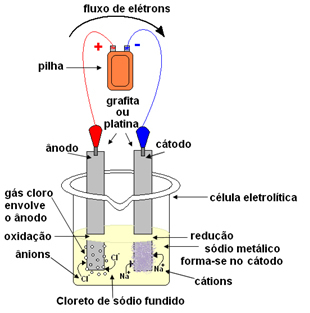
그런 다음 용융 된 염을 용기, 전해 용기에 넣고 두 개의 불활성 백금 또는 흑연 전극을 염화나트륨에 담근다. 이 전극은 배터리 또는 셀과 같은 직류 전류를 생성하는 소스에 연결됩니다.
전류가 흐르면 다음이 발생합니다.
- 배터리 또는 셀의 음극은 음극이되는 전극 중 하나에 전자를 공급합니다.
- 음극: 세포에서 전자를 받아 음극이되어 Na 양이온을 끌어 당깁니다.+, 반대 요금이 끌기 때문입니다. 이 이온은 전극 (음극)에서 전자를 받아 환원이 일어나 금속 나트륨을 형성합니다.
절감:에서+(ℓ) + 및- → 안으로(에스)
금속 나트륨은 전극 위에 증착되어 저장소로 보내집니다.
- 양극: 양전하를 띠고 Cl 음이온을 끌어 당깁니다.- (그것이 양극이라고 불리는 이유입니다). 이 이온은 양극과 접촉 할 때 전자를 잃어 버리고, 따라서 산화를 거쳐 염소 원자를 형성하며, 이는 즉시 두 개씩 결합하여 염소 가스를 형성합니다.
산화:2Cl-(ℓ) → 2 및- + 1Cl2(지)
이 가스는 양극 주변에서 버블 링되며 시스템에 적합한 유리관에 의해 수집됩니다.
따라서이 경우 발생하는 전체 반응은 다음과 같습니다.
음극: 2Na+(ℓ) + 2e- → 2Na(에스)
양극: 2Cl-(ℓ) → 2 및- + 1Cl2(g) ____________
글로벌 반응: 2Na+(ℓ) + 2Cl-(ℓ) → 2Na(에스) + 1Cl2(지)
주의해야 할 또 다른 중요한 측면은 언급 된 텍스트 (Igneous Electrolysis)의 끝 부분에 강조 표시되어 있습니다. 발생하는 경우 전류를 생성하는 데 사용되는 셀 또는 배터리는 ddp (전위차)가 전기차의 전위차보다 크거나 같아야합니다. 반응.
우리가 고려중인 염화나트륨 전기 분해의 경우를 살펴 보겠습니다. 이 반응의 전위차를 알아 내기 위해서는 음극의 표준 환원 전위를 양극의 전위차로 낮추면 충분합니다. 이것은 본문에 설명되어 있습니다. 배터리의 잠재적 인 차이 .
표준 감소 잠재력 표를 통해 (E0빨간색), 우리는 다음을 알고 있습니다.
에서+(ℓ) + 및- → 안으로(에스) 과0빨간색 = -2.71
2Cl-(ℓ) → 2 및- + 1Cl2(g) 그리고0빨간색 = +1.36
이제 글로벌 반응의 잠재적 인 차이를 알기 위해이 값을 줄이십시오.
∆ 그리고0 = 그리고0빨간색 (음극) -그리고0빨간색 (양극)
∆ 그리고0 = -2,71 – (+ 1,36)
∆ 그리고0 =-4.07V
따라서 염화나트륨의 화성 전기 분해를 수행하려면 사용할 셀 또는 배터리의 전압이 4.07V 이상이어야합니다.
음수 값은 자발적이지 않은 프로세스임을 나타냅니다.. 자발적인 과정 인 배터리의 경우 기전력 값 (∆E0) 항상 긍정적입니다.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/eletrolise-Ignea-cloreto-sodio.htm