영형 벤젠 다음으로 분류되는 유기 화합물입니다 방향족 탄화수소. 산업, 실험실 공정, 철강 회사 및 석유 화학 산업에서 정유를위한 원료로 널리 사용됩니다.
읽기: 메탄 — 가장 작고 단순한 탄화수소
공식
벤젠은 분자식의 화합물입니다 씨6H6그리고 누가 매우 안정적인 구조엘. 벤젠의 구조식은 다음과 같이 표시됩니다.
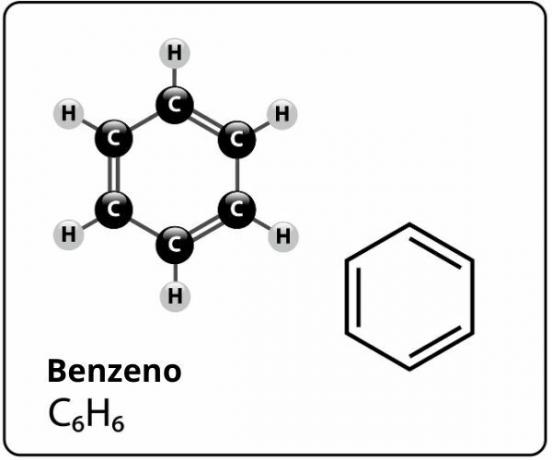
벤젠에 대해이 구조를 제안한 사람 6 개의 탄소 원자가 교대로 이중 결합으로 결합되어 있습니다. 육각형을 형성하고 그들 각각에 원자를 붙인 수소, 그것은 독일 화학자였습니다 프리드리히 아우구스트 케 쿨레, 1866 년.
벤젠은 공명, 탄소 사이의 결합에있는 전자의 위치가 다릅니다. 이러한 이유로 벤젠은 다음과 같이 나타낼 수 있습니다.
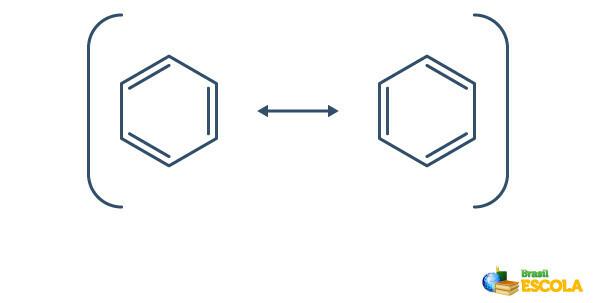
벤젠의 실제 구조는 위에 표시된 공명 구조 사이의 매개체입니다. 이것은 벤젠이 때때로 한 형태로, 때로는 다른 형태로 나타나거나 두 형태가 동시에 존재한다는 것을 말하는 것이 아닙니다. 우리는 다음과 같이 벤젠을 나타냅니다.
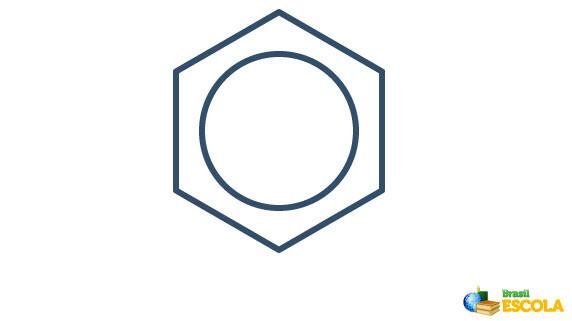
육각형 안의 원은 결합에서 전자 사이의 공명을 나타냅니다.
풍모
- 벤젠은 액체입니다 무색, 가연성 흔하다 기분 좋은 향기 특성.
- 분자식: C6H6.
- 몰 질량: 78.11 g / mol.
- 밀도: 0.876 g / cm³.
- 녹는 온도: 5.5 ° C.
- 끓는 온도: 80.1 ºC – 낮은 끓는 온도는 높은 휘발성을 설명합니다 (증발하기 쉬움).
벤젠은 독성 물질 그 증기는 현기증, 두통 및 실신을 유발할 수 있습니다.
읽기 :일산화탄소 — 극도로 독성, 무색, 무취 가스
벤젠의 응용 및 독성
벤젠은 주로 원료로 사용 플라스틱과 같은 다른 물질의 생산을위한 산업에서 폴리머 스티렌, 수지, 접착제, 나일론, 고무, 윤활유, 살충제 등을 기반으로합니다.
벤젠은 주로 실험실에서 극성과 극성을 가진 톨루엔으로 대체되었습니다. 용해도 벤젠과 비슷하지만 독성이 적고 끓는 온도가 높습니다.
벤젠은 다음 그룹에 속합니다. 발암 물질로 간주되는 화학 물질고농도로 장기간 노출되면 골수 및 백혈병에 손상을 입 힙니다. 단기적으로 벤젠은 현기증, 졸음, 빠른 심장 박동, 발작 및 실신을 유발할 수 있습니다.
벤젠은 휘발성 액체이기 때문에 가스를 쉽게 방출하므로 주로 호흡기를 통해 벤젠 오염이 발생합니다.
벤젠은 어디에서 발견됩니까?
환경으로 방출되는 대부분의 벤젠 인간 행동의 결과, 주로 산업 활동에서 발생하지만 화재 및 화산 활동의 부산물로 방출 될 수도 있습니다.
벤젠은 구성 물질 중 하나 석유 가솔린에 존재하며 자동차 연료를 태워 대기로 방출됩니다. 또한 청량 음료와 담배에서도 발견됩니다.

극성
벤젠은 비극성 분자, 다른 사람들과 마찬가지로 탄화수소 따라서 선물 물에 대한 매우 낮은 용해도 (15 ° C에서 0.8g / L). 일부 실험실 절차에서 벤젠은 비극성 물질의 유기 용매로 사용됩니다.
명명법
방향족 화합물의 명명법, 즉 구조에 벤젠이있는 것에 만 적용되는 규칙이 있습니다. 이 규칙은 벤젠 고리에 부착 된 라디칼의 양에 따라 두 가지 경우로 나뉩니다.
첫 번째 사례: 벤젠 고리에 라디칼이 하나만 붙어있는 경우 다음 규칙에 따라 이름이 지정됩니다.
라디칼 이름 + 벤젠
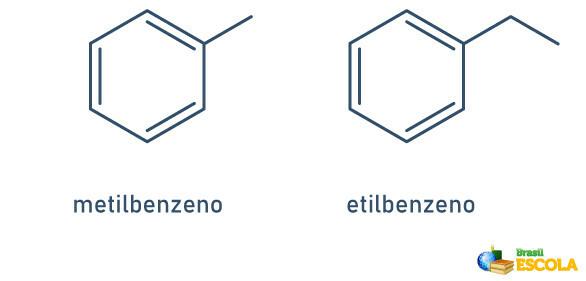
스템의 위치를 표시 할 필요는 없습니다.
두 번째 사례: 벤젠에 하나 이상의 라디칼이 부착 된 경우 이름은 다음 규칙을 따릅니다.
방사형 위치 + 방사형 이름 + 벤젠
예를 참조하십시오.

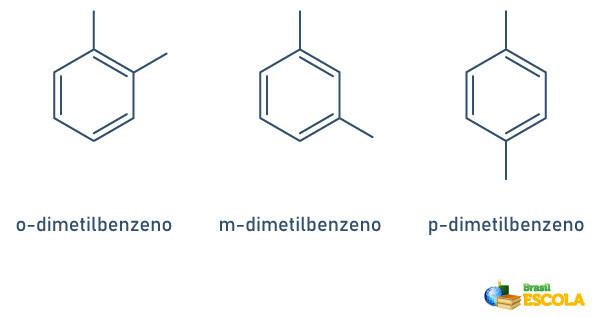
벤젠 고리에 부착 된 라디칼이 두 개 뿐인 경우 사용할 수있는 특정 명명법이 있습니다.
- 1,2 또는 ortho (o);
- 1.3 또는 목표 (m);
- 1.4 또는 ~ (p).
예를 참조하십시오.
읽기: 질산 암모늄 — 폭발물 제조에 사용되는 반응성이 높은 화합물
호기심
- 벤젠은 국제기구에 의해 분류되는 극도로 발암 성 물질입니다. 암 연구팀, 그룹 1, 담배, 디젤 연기 및 육류 처리되었습니다.
- 여러 국가에서 벤젠의 노출 및 배출을 제한하는 여러 규제 기관이 있습니다. 브라질에서이 역할은 Anvisa의 책임입니다.
- 벤젠은 위험을 알기 전에 기분 좋은 냄새 때문에 애프터 쉐이브와 같은 화장품에 사용되었습니다.
작성자: Victor Ricardo Ferreira
화학 교사
