알칸의 설 폰화 반응 그들은 유기 치환 반응, 생산을 목표로 수행 술폰산 (SO 그룹을 갖는 유기 화합물3탄소 원자 또는 탄소 사슬에 부착 된 H) 및 물 (H2영형).
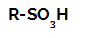
술폰산의 구조식
술 폰화 반응을 수행하기 위해 알칸, 우리는 알칸 (탄소와 수소 원자로 만 포화 된 탄소 사슬로 형성된 화합물)과 황산 (H2뿐4) 농축, 가열 (∆).
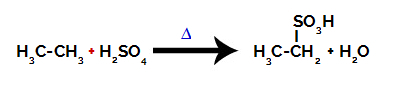
2- 탄소 알칸의 술 폰화를 나타내는 화학 방정식
알칸에서 설 폰화 반응의 원리
같은 알칸 설 폰화 반응 그것은 치환 반응입니다. 우리는 그 안에 더 작은 성분들 사이의 교환이 있습니다. 전기 음성도 반응물, 즉 알칸과 황산 사이. 알칸에는 수소와 황산, 술폰 기가 있습니다.
아래에 우리는 알칸의 술 폰화 반응. 예를 들어, 우리는 가장 단순한 알칸 인 메탄 (CH4):
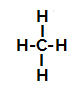
메탄의 구조식
1 단계 : 황산에서 수산기 (OH)와 황 (S) 사이의 결합 중단.
황산에 존재하는 각 하이드 록실 그룹은 전기 음성이 더 강한 것이 특징입니다. 반응 중 가열하면 수산기와 황 사이의 결합이 끊어지는 경향이 있습니다.
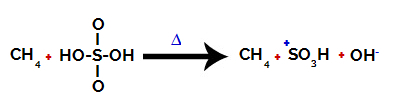
유황과 수산기의 결합 파괴
그러나 구조의 전자적 재 배열로 인해 모든 수산기의 결합이 끊어지는 것은 아닙니다. 수산화 음이온 (OH)이 얻어진다.-) 및 술폰 양이온.
2 단계 : 알칸 분자에 대한 하이드 록실 그룹 공격.
그런 다음 히드록시기 (OH-) 알칸에 대한 공격을 수행하여 탄소와 수소 사이의 결합 (전기 음성도의 차이로 인해 더 취약 함)이 끊어지게합니다.
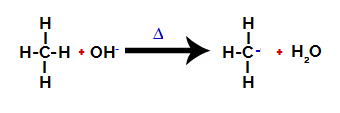
알칸에서 탄소와 수소 사이의 결합 끊기
노트 : 탄소와 수소 사이의 결합 파괴는 전자 밀도 또는 전하가 낮은 탄소에서 항상 가장 자주 발생합니다. 탄소의 수소가 적거나 더 많은 그룹이 결합 될수록 전자 밀도가 낮아집니다. 그래서 우리는 :
3 차 탄소 <2 차 탄소 <1 차 탄소
결합이 끊어지면 알칸은 전자가 부족한 탄소 (탄 양이온)가됩니다. 수산화기 (OH)-) 방출 된 수소와 상호 작용하여 물 분자를 형성합니다.
3 단계 : 술폰기에 형성된 라디칼의 공격.
마지막으로, 술폰 기는 나머지 알칸에 의해 공격을 받아 술폰산을 형성합니다.
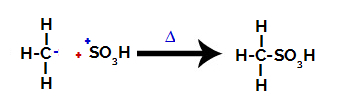
상호 작용하고 술폰산을 형성하는 구조
알칸의 설 폰화 반응을 나타내는 방정식의 예
첫 번째 예 : 프로판의 설 폰화.
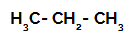
프로판의 구조식
프로판에는 2 개의 1 차 탄소와 1 개의 2 차 탄소가 있는데, 이들은 서로 다른 양의 수소에 결합되어 있기 때문에 전하가 다릅니다. 탄소는 수소보다 전기 음성이 높기 때문에 이러한 탄소는 전자 밀도가 다릅니다.
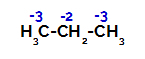
프로판의 각 탄소 원자에 대한 전하 분포
1 차 탄소에서 전하는 -3 (수소 3 개에 결합되어 있기 때문에)이고 2 차 탄소에서는 전하가 -2 (수소 2 개에 결합되어 있기 때문에)입니다. 따라서 탄소와 수소, 때로는 탄소 1 (한 분자의), 때로는 탄소 2 (다른 분자의) 사이의 결합이 끊어집니다.
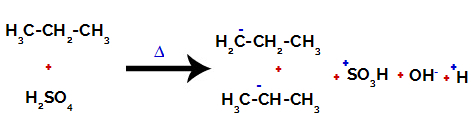
다른 탄소에서 탄소와 수소 사이의 결합 끊기
황산과 알칸 모두에서 결합 사이의 단절 후, 탄소 1의 수소를 술폰 그룹으로 대체 한 제품이며 탄소에서도 동일하게 발생합니다. 2.
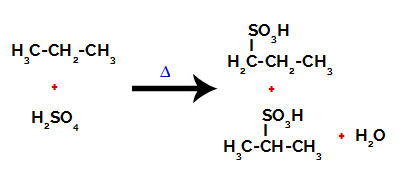
프로판의 술폰 화로 형성된 제품
두 번째 예 : 2- 메틸-부탄의 설 폰화.

2- 메틸-부탄의 구조식
2- 메틸-부탄에는 3 개의 1 차 탄소, 2 차 탄소 및 3 차 탄소가 있습니다. 다음 구조에서 볼 수 있듯이 다른 전하 및 결과적으로 다른 전자 밀도 :
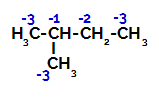
2- 메틸-부탄의 전자 전하 분포
따라서 2- 메틸-부탄에는 탄소와 수소 사이의 결합을 끊을 수있는 몇 가지 가능성이 있습니다. 탄소 1 (분자의), 탄소 2 (다른 분자의), 탄소 3 또는 탄소에서 발생할 수 있습니다. 4. 그러나 탄소수 2의 붕괴가 더 흔하다는 것은 주목할 만하다.
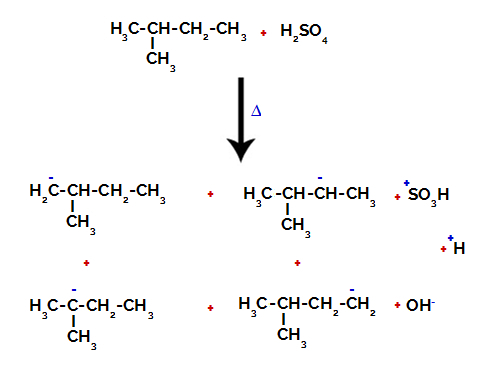
다른 탄소에서 탄소와 수소 사이의 결합 끊기
황산과 알칸 모두에서 결합 사이의 파손 후 탄소 1의 수소를 술폰기로 대체 한 제품이며, 탄소 2.

2- 메틸-부탄의 술폰 화로 형성된 제품
나로. Diogo Lopes Dias
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/reacoes-sulfonacao-alcanos.htm

