이 텍스트에서 우리는 차트 신체 상태의 변화 아무에게나 순수한 물질, 이러한 유형의 다이어그램을 해석하는 방법 및 혼합물의 그래프가 표시되는 방법.
이를 위해 물의 예를 생각해 봅시다. -10ºC의 온도에서 얼음 한 잔을 가져다가 1 기압의 압력에서 가열 과정을 시작한다고 상상해보십시오. 온도가 -10ºC에서 -9ºC로, -8ºC로 올라가면 얼음은 0ºC의 온도에 도달 할 때까지 고체 상태를 유지합니다.
이 시점에서 액체 상태로 변화하기 시작합니다. 즉, 융합이 시작됩니다. 온도는 이전처럼 계속 상승하지 않지만 모든 얼음이 녹을 때까지 0 ° C에서 일정하게 유지됩니다.

모든 고체를 녹인 후 시스템의 온도는 100 ° C에 도달 할 때까지 계속 상승합니다. 이 온도에서 액체 상태에 있던 물은 증기 상태로 바뀌기 시작합니다. 즉 끓을 것입니다.
에서 일어난 것처럼 융합 점끓는점에서 모든 액체가 증기로 변할 때까지 온도도 일정하게 유지됩니다. 그 후 시스템을 계속 가열하면 온도가 계속 상승합니다.
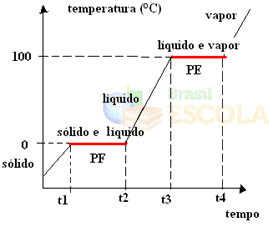
준비된! 이것은 물의 물리적 상태 또는 가열 곡선의 변화를 나타내는 그래프 또는 다이어그램입니다. 역 과정이라면 다음과 같은 수냉 곡선을 갖게됩니다.
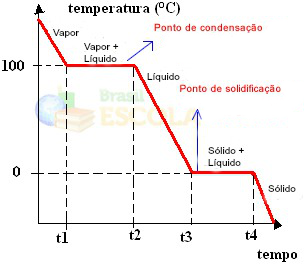
이 그래프의 매우 중요한 측면은 두 단계로 구성된다는 것입니다. 즉, 온도가 한동안 일정하게 유지되는 두 지점이 있습니다. 이것은 항상 순수한 물질의 상태 변화에서 발생합니다. 유일한 차이점은 녹는 점과 끓는점 값입니다.
예를 들어 물과 달리 산소는 액체가 아니라 실온 (약 20ºC)의 가스입니다. 이는 해수면에서 녹는 점이 -223.0 ° C이고 끓는점이 -183.0 ° C이기 때문입니다. 신체 상태 변화 차트를 참조하십시오.

일반적인 믹스 그래픽
혼합물을 가열하거나 냉각하는 경우 녹는 점과 끓는점은 즉, 그래프에서 관찰되는 두 수준이 형성되지 않습니다. 위.
물리적 상태의 변화는 고정 된 양이 아닌 온도 범위에서 발생합니다. 예를 들어 녹는 점은 주어진 온도에서 시작하여 다른 온도에서 끝납니다. 다음 그래프와 같이 끓는점에서도 마찬가지입니다.
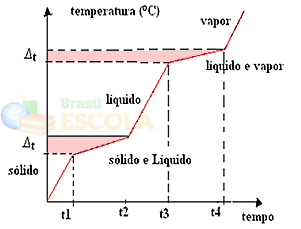
두 가지 예외는 공융 및 공비 혼합물입니다. 그들에게 무슨 일이 일어나는지보십시오 :
a) 공융 혼합물
공융 혼합물은 융합하는 동안 순수한 물질 인 것처럼 행동합니다. 즉, 그 시점에서 온도는 응집 상태 변화의 시작부터 끝까지 일정하게 유지됩니다.

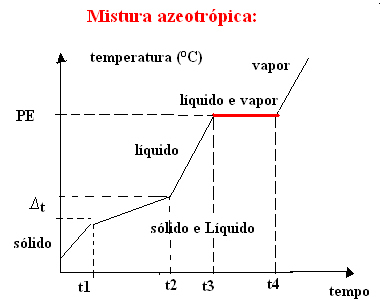
b) 공비 혼합물
공비 혼합물은 끓는 동안 순수한 물질처럼 행동합니다. 즉, 이 시점에서 온도는 응집 상태 변화의 시작부터 끝까지 일정하게 유지됩니다.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm

