영형 루미놀 분자식이 C 인 분말 유기 화합물8H7영형2엔3. 이 화학 시약은 과산화수소 (H2영형2, 그 용액은 과산화수소라고 함), 일부 수산화물 및 기타 화학 물질은 액체 용액을 생성합니다.
루미놀과 과산화수소가 반응하면 파란색 형광등이 방출됩니다. 그러나이 반응은 매우 느리기 때문에 둘의 혼합물만으로는 관찰 할 수 없습니다. 반면에 혈액과 접촉하면 헤모글로빈의 철은 촉매 역할을하여이 반응을 가속화하며, 복사 광이 나타나는 데 5 초 밖에 걸리지 않습니다. 따라서 루미놀 용액을 피가 섞인 곳에 분사하면 화학 발광이 관찰됩니다.
루미놀의 화학 구조를보십시오 :
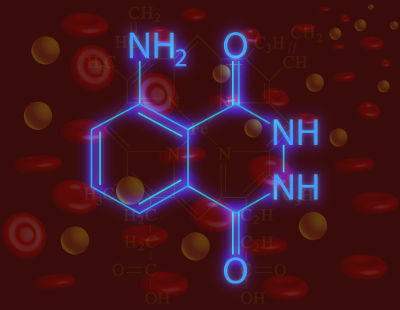
순수 루미놀의 구조식
Luminol은 범죄 현장에서 혈액을 식별하기 위해 법의학에서 널리 사용됩니다. 옷, 카페트 등과 같은 장소 또는 기타 품목을 전에 세탁 한 적이 있더라도 섬유는 직물의 일부는 철 화합물의 일부를 흡수하지만 장소는 사용에 의해 "조명" 루미놀. 어두운 곳에서는 피가 있음을 나타내는 파란색 점을 명확하게 볼 수 있습니다.
용어 "화학 발광"은 빛을 생성하는 화학 반응을 나타내는 데 사용됩니다. 이것이 바로 루미놀과 과산화수소 사이의 산화 반응에서 일어나는 일입니다. 루미놀은 질소와 수소 원자를 잃고 산소 원자를 얻어 3- 아미노 프탈레이트를 형성합니다. 이 화합물의 전자는 반응물보다 높은 에너지 수준에 있으며 불안정한 상태이므로 전자는 에너지 상태로 돌아갑니다. 낮은, 가시 전자기파의 형태, 즉 우리가 색 파장 범위에서 볼 수있는 빛의 형태로 여분의 에너지를 방출합니다. 푸른.
Luminol은 일반적으로 범죄 현장에서 다른 증거를 파괴 할 수 있으므로 전문가가 다른 옵션을 고려한 후에 만 범죄 현장에 뿌려집니다. 또한 고려해야 할 한 가지 측면은 루미놀을 "광택"시키는 것은 혈액뿐 아니라 표백제와 같은 다른 화합물도 있다는 것입니다. 따라서 조사관은 그것이 실제로 인간의 혈액인지 확인하기 위해 추가 검사를 수행해야합니다.
루미놀은 위에서 설명한 바와 같이 금속 표면에 뿌려 질 수 없습니다. 파란색을 나타내는 반응을 촉매하는 것은 철입니다. 따라서 이러한 표면의 철분은 위양성 결과를 가져올 수 있습니다.
* 이미지 크레딧: 저자: 모두가 유휴 /Fonte: 위키미디어 공용.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-luminol.htm

