이중 소금 분류 중 하나에 주어진 이름입니다. 무기 염 받을 수 있습니다. 다른 분류는 단순, 명반, 수산화, 수소화 그리고 수화. 이중 염으로 특성화 되려면 무기 염은 아래에 설명 된 조합 중 하나를 가져야합니다.
양이온 (Y)과 2 개의 음이온 (X 및 W)은 다음 공식으로 표시됩니다.
YXW
음이온 (X)과 두 양이온 (Y 및 Z)은 다음 공식으로 표시됩니다.
YZX
노트 : 이 염은 중화 반응 둘 사이에 수행됩니다 기지 다르고 하나 산, 또는 두 개의 다른 산과 염기 사이.
이중 솔트에 대한 명명 규칙
이름을 이중 소금아래에서 볼 수 있듯이 각 유형의 이중 소금에 대해 특정 명명 규칙이 있기 때문에 먼저 그 구성을 알아야합니다.
a) 두 개의 양이온을 가진 이중 소금에 대한 명명 규칙
하나 이중 소금 두 개의 양이온이있는 경우 다음 규칙을 사용해야합니다.

2 개의 양이온이있는 이중 염에 사용되는 명명 규칙
다음은이 명명 규칙을 적용한 두 가지 예입니다.
첫 번째 예 : 선4에스
이 소금은 다음으로 구성됩니다.
음이온: 황화물 (S-2);
더 많은 전기 양성 양이온: 리튬 (Li+1);
덜 전기 양성 양이온: 암모늄 (NH4+1).
따라서 그 이름은 리튬 (이중) 황산 암모늄입니다.
두 번째 예 : RbCaBO3
이 소금은 다음으로 구성됩니다.
음이온: 붕산염 (BO3-3);
더 많은 전기 양성 양이온: 루비듐 (Rb+1);
덜 전기 양성 양이온: 칼슘 (Ca+2).
따라서 그 이름은 루비듐과 칼슘의 붕산염 (이중)입니다.
b) 2 개의 음이온을 갖는 이중 염에 대한 명명 규칙
하나 이중 소금 두 개의 음이온이있는 경우 다음 규칙을 사용해야합니다.
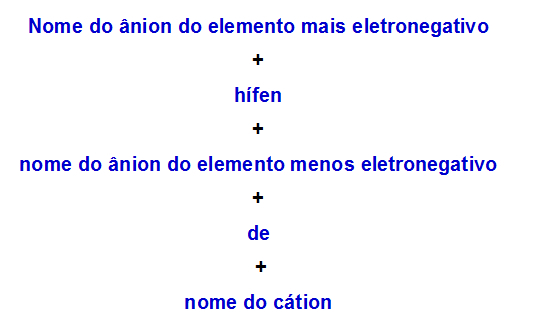
두 개의 음이온이있는 이중 염에 사용되는 명명 규칙
다음은이 규칙을 적용하는 두 가지 예입니다.
첫 번째 예 : MgFI
이 소금은 다음으로 구성됩니다.
양이온: 마그네슘 (Mg+2);
대부분의 전기 음성 음이온: 불소 (F-1);
덜 전기 음성 음이온: 요오드화물 (I-1).
따라서 그 이름은 마그네슘 불화물-요오드화물입니다.
두 번째 예 : ZnNO2br
이 소금은 다음으로 구성됩니다.
양이온: 아연 (Zn+2);
더 많은 전기 음성 음이온: 아질산염 (NO2-1);
덜 전기 음성 음이온: 브롬화물 (Br-1).
따라서 그 이름은 아질산 아연입니다.
명명법에서 이중 소금의 공식 조립
a) 두 개의 양이온이있는 이중 염의 경우
공식의 구성 이중 소금 그것은 모든 소금에서와 같이 표준화 된 이름, 즉 먼저 양이온과 음이온을 아는 것에 달려 있습니다. 이중 소금은 두 개의 양이온을 가질 수 있으므로 공식에서 순서와 배치는 주어진 이름을 따릅니다.
첫 번째 예 : 바륨 니켈 피로 인산염 II
이 염에는 인산염 (P2영형7), 바륨 (Ba+2) 및 니켈 II (Ni+2), 그 순서로 쓰여진 양이온. 공식은 BaNiP입니다.2영형7.
두 번째 예 : 구리 II 인산염 및 금 I
이 염에는 인산염 (PO4-3), 구리 II (Cu+2) 및 금 I (Au+1), 그 순서로 쓰여진 양이온. 따라서 공식은 CuAuPO입니다.4.
b) 두 개의 음이온이있는 이중 염의 경우
의 경우 이중 소금 두 개의 음이온으로, 우리는 또한 공식에 음이온을 넣을 때 주어진 이름에 나타나는 순서를 따릅니다.
첫 번째 예 : 황산 니켈-요오드화물 III
이 염에는 황산 음이온 (SO4-2) 및 요오드화물 (I-1), 그리고 니켈 III 양이온 (Ni+3). 그래서 그 공식은 NiSO입니다4나는.
두 번째 예 : 납 시안화물 인산염 IV
이 염에는 인산 음이온 (PO4-3) 및 시안화물 (CN-1),이 순서로 작성되고 납 양이온 IV (Pb+4). 그래서 그 공식은 PbPO입니다4CN.
나로. Diogo Lopes Dias
출처: 브라질 학교- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm
