전자를 공유함으로써 공유 결합을 수행하는 화합물의 물리적 및 화학적 특성에 대한 분석은 이러한 물질간에 큰 차이가 있음을 보여줍니다. 그러나 이러한 특성 자체를 살펴보기 전에 분자 물질과 공유 물질의 차이점을 살펴 보겠습니다.
에서 분자 물질 이들은 원자가 공유 결합을 통해 연결되어 결정된 수의 분자를 생성 할 때 형성되는 것들입니다.
그러나 공유 결합은 매우 크고 불확실한 원자 수를 가진 네트워크 구조에서 화합물을 생성 할 수도 있습니다. 거대 분자. 이러한 물질은 공유 화합물 또는 공유 네트워크 고체. 이러한 화합물의 예로는 다이아몬드 (C), 흑연 (C), 이산화 규소 (SiO2) 및 실리콘 카바이드 (SiC).
이제 주요 속성을 살펴 보겠습니다.
- 실온에서의 물리적 상태 : 주변 조건에서 분자 및 공유 화합물이 발견됩니다. 세 가지 물리적 상태에서 (고체, 액체 및 기체).
예 :
영형 고체: 설탕 (자당), 실리카 (모래), 다이아몬드, 흑연;
영형 액체: 물, 아세톤, 에탄올;
영형 텅빈: 황화수소, 염소 가스, 브롬 가스, 수소 가스.

- 녹는 점과 끓는점 : 일반적으로 이러한 물질의 녹는 점과 끓는점은 이온 성 물질보다 작음.
공유 물질은 분자 물질보다 끓는 온도가 높으며 항상 1000 ° C 이상입니다. 분자가 더 밀접하게 결합되어 결정 격자를 형성함에 따라 상태를 변화 시키려면 더 많은 에너지를 제공해야하기 때문입니다.
공유 및 분자 화합물의 끓는점과 융점을 방해하는 두 가지 요인: a 몰 질량 그리고 분자간 힘.
몰 질량이 클수록 분자의 관성이 커지고 결과적으로 끓는점과 융점이 높아집니다. 몰 질량이 근사치이면 분자간 힘을 봅니다. 가장 강한 분자간 힘은 수소 결합의 힘으로 더 높은 끓는점과 융점으로 이어집니다. 중간체는 영구 쌍극자이고 가장 약한 것은 끓는점과 융점이 낮아지는 유도 쌍극자입니다.
- 전류: 순수한 형태로 액체와 고체는 모두 전류를 전도하지 않습니다.
이중 결합 전자가 공명하여 특정 이동성을 갖기 때문에 고체 형태로 전류를 전도하는 흑연은 예외입니다.
- 용해도 : 극성은 극성으로 용해되고 비극성은 비극성으로 용해됩니다.
- 끈기: 충격이나 기계적 충격에 대한 공유 물질의 내성이 낮습니다. 일반적으로 유리의 경우와 같이 규산 나트륨과 칼슘에 의해 형성되는 깨지기 쉬운 고체입니다.

- 인성: 일반적으로 경도가 높습니다. 흑연을 제외하고는 탄소 원자가 다른 세 개의 탄소 원자와 연결되어 특정 이동성을 가진 육각형 판을 형성하여 부드럽습니다. 이 때문에 윤활제로도 사용됩니다.
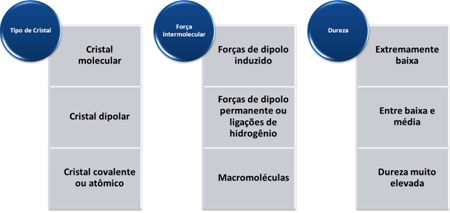
이 물질의 경도는 아래 표와 같이 결정의 유형에 따라 다릅니다.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm
