이온 결합은 이름에서 알 수 있듯이 이온 사이에서 발생합니다. 그들은 반대 전하를 가지기 때문에 양이온 (양전하를 가진 원소)과 음이온 (음전하를 가진 원소)이 서로 정전 기적으로 끌어 당겨 결합을 형성합니다. 그러나 이온 성 고체는 격자 또는 결정 격자라고하는 잘 정의 된 기하학적 모양으로 구성된 양이온과 음이온의 응집체로 구성됩니다.
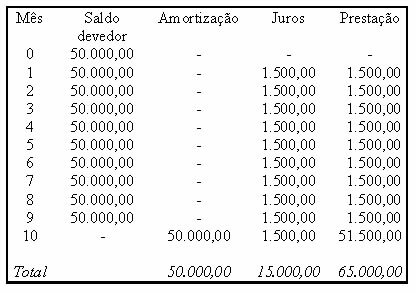
예를 들어, 소금 (염화나트륨)은 전자가 나트륨에서 염소로 최종적으로 전달되어 나트륨 양이온 (Na+) 및 염화 음이온 (Cl-). 실제로이 반응은 두 개의 원자뿐만 아니라 아래 그림과 같이 입방체 모양의 결정 격자를 형성하는 엄청나고 불확실한 수의 원자를 포함합니다.
주사 전자 현미경으로 소금 결정을 보면, 내부 구조 때문에 실제로 입방체임을 알 수 있습니다.

그러면 모든 이온 화합물이 불확정하고 매우 많은 수의 이온으로 구성되어 있기 때문에 이온 화합물을 어떻게 나타낼 수 있습니까?
일반적으로 사용되는 공식은 단위 공식, 그것은 화합물의 총 전하가 중화되도록 결정 격자를 구성하는 양이온과 음이온의 가능한 최소 수로 표현되는 비율을 나타냅니다.. 이것이 일어나기 위해서는 원자가 포기한 전자의 수가 다른 원자가받는 전자의 수와 같아야합니다.
이온 화합물의 단위 식에 대한 몇 가지 측면이 중요합니다.
- 항상 양이온을 먼저 쓴 다음 음이온을 쓰십시오.
- 모든 이온 화합물은 전기적으로 중성이므로 개별 이온 전하를 기록 할 필요가 없습니다.
- 각 이온의 오른쪽에 나타나는 아래 첨자 번호는 양이온과 음이온의 원자 비율을 나타냅니다. 이 숫자를 인덱스라고하며 숫자 1은 쓰지 않습니다.
예를 들어, 염화나트륨의 경우 각 염화물 음이온에 대해 정확히 1 개의 나트륨 양이온이 있으므로 단위 공식은 NaCl입니다.
다른 예보기, Al3+ 세 개의 양전하가있는 반면 F- 그것은 단지 하나의 부정적인 것을 가지고 있기 때문에 화합물을 중화시키기 위해서는 3 개의 불소 음이온이 필요합니다. 따라서 단위 공식은 AlF3.
이온 화합물의 단위 공식에 도달하는 간단한 방법은 아래의 일반적인 방법에 표시된 것처럼 전하를 인덱스로 교환하는 것입니다.
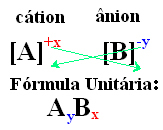
예 :

이온 성 물질을 나타내는 데 사용되는 또 다른 공식은 루이스 공식 또는 전자 공식, 뭐 요소 기호 주변의 "공"이온의 원자가 쉘에서 전자를 나타냅니다. 소금의 경우 :

작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/formulas-para-representar-as-ligacoes-ionicas.htm