공유 결합은 두 원자가 전자 배열을 획득하기 위해 전자 쌍을 공유 할 때 발생합니다. 귀금속 (가가 쉘에 8 개의 전자가 있거나 K 쉘만있는 경우에는 2 개가 있음), 규칙에 따라 팔중주.
그러나 공유 결합의 특별한 경우가 있습니다. 공유 전자 쌍은 이미 안정된 원자 중 하나에서만 발생합니다.. 이전에는 이러한 유형의 공유 결합을 여격, 오늘날 더 일반적으로 동등 어구.
이것이 어떻게 발생하는지 이해하려면 몇 가지 예를 참조하십시오.
- CO (일산화탄소) :
탄소는 원자가 껍질에 4 개의 전자를 가지고 있습니다. 따라서 옥텟 규칙에 따라 안정되기 위해서는 총 8 개의 전자 4 개를 더 받아야합니다. 반면에 산소는 원자가 껍질에 6 개의 전자를 가지고 있으며, 고귀한 가스 네온의 구성을 유지하려면 2 개의 전자를 받아야합니다.
따라서 먼저 탄소와 산소는 두 쌍의 전자를 공유하여 산소가 안정적입니다.
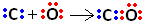
그러나 탄소는 여전히 6 개의 전자를 가지고 있고 2 개가 필요하기 때문에 불안정한 상태로 남아 있습니다. 따라서 이미 안정된 산소는 전자 쌍 중 하나를 탄소와 공유합니다. 즉, 산소와 dative 결합을 만들어 안정적으로 만듭니다.

좌표 공유 결합은 공통 공유 결합처럼 대시로 나타낼 수 있습니다.
- 뿐2 (이산화황) :
각 황과 산소 원자는 원자가 껍질에 6 개의 전자를 가지고 있으므로 각각 2 개의 전자를 받아야합니다. 처음에 황은 두 개의 공통 공유 결합을 만들어 산소 원자 중 하나와 두 쌍의 전자를 공유하며 둘 다 8 개의 전자로 안정적으로 유지됩니다.
그러나 다른 산소 원자는 안정적이지 않으므로 황은 배위 또는 dative 공유 결합을 통해 전자 쌍을 공유합니다.
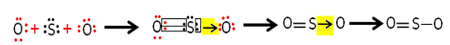
이 경우 분자에 세 개의 원자가 있으므로 한 원자에서 다른 원자로 결합이 이동할 수 있습니다. 이산화황 분자는 다음과 같이 나타낼 수도 있습니다. O ─ S = O.
우리는이 결합 현상을 공명. 아래 표에서 세 가지 예를 더 참조하십시오.
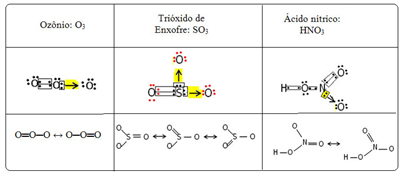
가능한 구조는 공명 구조 또는 정식 형식.
이러한 유형의 결합은 하이드로 늄 이온 (H)의 경우처럼 이온 형성에서도 발생합니다.3영형+) 및 암모늄 (NH4+).
첫째, H 양이온+ 그것은 수소가 단일 전자를 잃을 때 형성되어 양전하를 남깁니다. 따라서 안정되기 위해서는 두 개의 전자를 받아야합니다. 이것은 물 (하이드로 늄 이온의 경우) 및 암모니아 (암모늄 이온의 경우)와의 dative 결합을 통해 발생합니다. 손목 시계:

작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/ligacao-covalente-dativa-ou-coordenada.htm

