하나 치환 반응 두 가지 다른 시약의 구성 요소 간의 교환을 기반으로합니다. 안정성이 더 큰 화합물 (포화, 즉 탄소 사이에 단순한 결합 만 있음)은이 과정을 거칠 가능성이 더 큽니다. 그러나 벤젠도 가능합니다.
우리는 구조에서 벤젠 3 개의 이중 결합 (3 개의 파이 결합)이 있습니다. 즉, 이 화합물은 불포화 상태이지만 이러한 이중 결합은 항상 공명 현상 (3 개의 파이 결합의 위치 교대)을 겪습니다. 이러한 이유로 결합이 모든 탄소를 통과하기 때문에 구조의 안정성이 더 큽니다.
벤젠에서 발생할 수있는 치환 반응은 다음과 같습니다.
할로겐화;
질화;
설 폰화;
알킬화;
아 실화.
a) 할로겐화
이 반응에서 벤젠은 할로겐 (Br2, Cl2 야2), 항상 촉매가 존재하며 무기 염 (AlCl3, FeCl3 및 FeBr3). 이 과정은 벤젠 수소를 할로겐 원자로 교환하는 과정에서 발생합니다. 결과는 유기 할로겐화물의 형성 및 할로겐화 수 소화물. 예를 참조하십시오.
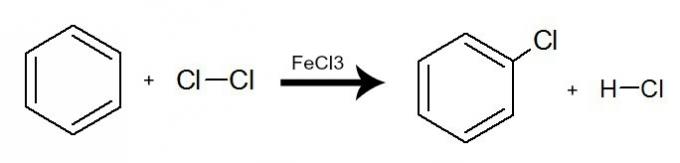
분자 염소 (Cl)를 사용하여 벤젠의 할로겐화를 나타내는 방정식2)
b) 질화
이 반응에서 벤젠은 질산 (HNO3), 항상 황산 촉매 (H2뿐4) 및 가열. 이 과정은 벤젠에서 수소를 NO 그룹으로 교환하는 과정에서 발생합니다.2 산의. 결과는 형성 니트로 화합물 그리고 물.
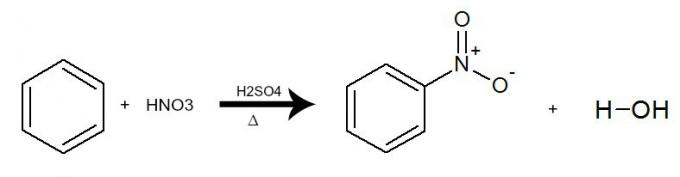
질산을 사용하여 벤젠의 질화를 나타내는 방정식
c) 설 폰화
이 반응에서 벤젠은 황산 (H2뿐4), 항상 삼산화황 촉매 (SO3) 및 가열. 이 과정은 SO 그룹에 의한 벤젠의 수소 교환으로 발생합니다.3산의 H. 결과는 형성 산 설 포닉 그리고 물.
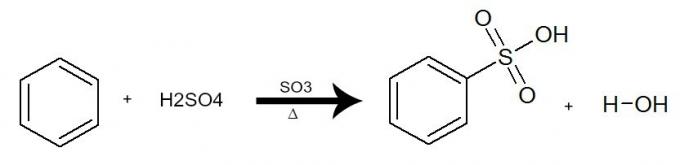
황산을 사용한 벤젠의 술 폰화를 나타내는 방정식
d) 알킬화
이 반응에서 벤젠은 유기 할로겐화물 (R-X), 항상 존재하는 촉매 삼염화 알루미늄 (AlCl3) 및 가열. 이 과정은 할로겐화물의 R 그룹 (유기 치환기)에 의해 벤젠에서 수소가 교환되면서 발생합니다. 결과는 분 지형 방향족 탄화수소의 형성및 무기산 (HX).
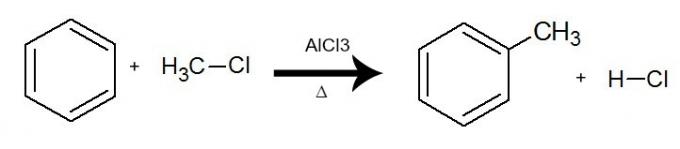
염소 메탄을 사용한 벤젠의 알킬화를 나타내는 방정식
e) 아 실화
이 반응에서 벤젠은 ethanoyl chloride로 나타낼 수있는 acid halide와 상호 작용합니다.
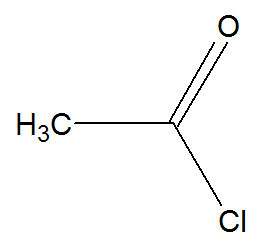
ethanoyl chloride의 구조식
반응은 촉매 삼염화 알루미늄 (AlCl3) 전체 산 할로겐화물 그룹에 대해 벤젠에서 하나의 수소가 교환됩니다 (X- 할로겐 제외). 결과는 형성 케톤 및 무기산 (HX). 예를 참조하십시오.
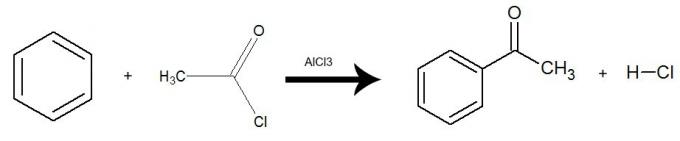
ethanoyl chloride를 사용하여 벤젠의 아 실화를 나타내는 방정식
나로. Diogo Lopes Dias
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/reacoes-substituicao-no-benzeno.htm

