분자간 힘 중에서, 유도 쌍극자 유도 쌍극자 힘 그것들은 네덜란드 물리학자 Johannes Diederik Van der Waals(1837-1923)에 의해 연구되지 않은 유일한 것들입니다. 그들은 독일 물리학자 Fritz Wolfgang London(1900-1954)에 의해 설명되었으므로 이러한 힘을 런던군 또는 런던 분산력. 이 힘에 부여된 또 다른 이름은 순간 쌍극자 유도 쌍극자.
이러한 힘은 다음에서 발생합니다. 비극성 물질, 예를 들어 H2, O2, F2, Cl2, CO2, CH4 및 C2H6 등. 그리고 그들은 또한 다음 사이에 발생할 수 있습니다 희가스 원자, 접근할 때 전기권 사이에 반발을 일으킵니다. 이와 같이 음전하 결핍으로 인해 전자가 음으로 극성화된 특정 면에 축적되고 반대 면에 양으로 축적됩니다.
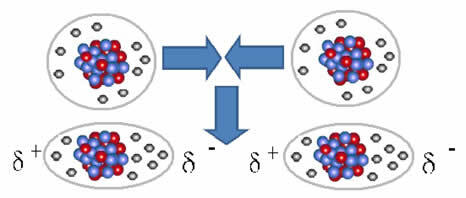
비극성 분자는 극이 없기 때문에 매우 멀리 떨어져 있고 상호 작용이 없는 기체 상태에서 액체 및 고체 상태로 이동할 수 있습니다. 이러한 응집 상태에서 분자는 더 가깝고 전자와 전자 사이의 전자 인력 또는 반발력 핵은 일시적으로 양극과 음극을 발생시키는 전자 구름의 변형을 유발할 수 있습니다. 일시적인.
순간 쌍극자는 이웃 분자의 분극을 유도하여 인력을 유발할 수 있습니다.
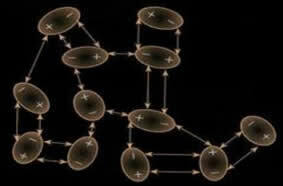
이 유도도 발생할 수 있습니다. 서로 다른 분자 사이 그리고 일반적으로 이 힘은 강도가 약하다 쌍극자-쌍극자 및 수소 결합 강도보다 따라서 고체 상태인 드라이아이스(이산화탄소-CO2) 및 요오드(I2)와 같이 이러한 상호작용 강도를 갖는 고체는 승화(기체 상태로 이동); 상호 작용을 방해하는 데 필요한 에너지가 작기 때문입니다.
극성 분자와 비극성 분자 사이의 분자간 힘의 예는 산소 가스(무극성)와 물(극성) 사이에서 발생합니다. 물의 음의 끝 부분이 O2에 접근하여 자체 반발하여 비극성 분자의 전자 구름이 멀어지는 것으로 나타났습니다. 그런 다음 산소는 순간적으로 분극되어 물과 상호 작용하기 시작하여 물에 용해됩니다.
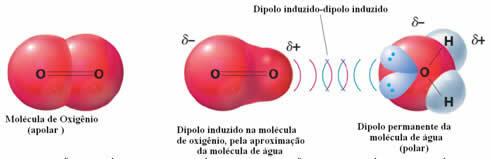
이러한 힘이 약하기 때문에 이 기체의 물에 대한 용해도는 작습니다. 그럼에도 불구하고 다양한 수생 생물의 생명을 보존하기 위해서는 그 존재가 필수적입니다.
이 상호 작용력은 자연에서도 발생하여 도마뱀붙이의 발과 도마뱀붙이가 걷는 표면 사이에 접착력을 제공합니다. 그렇기 때문에 넘어지거나 달라붙지 않고 벽과 천장을 걸을 수 있습니다.
제니퍼 포가사
화학과 졸업
브라질 학교 팀
원천: 브라질 학교 - https://brasilescola.uol.com.br/quimica/forcas-dipolo-induzido-dipolo-induzido-ou-dispersao-london.htm

