산화 원자, 그룹 또는 이온 종에 의한 전자 손실 과정에 주어진 이름 화학 반응. 의 증가로 확인된다. 녹스 (산화수) 반응물과 생성물을 비교할 때 종 또는 원자.
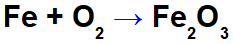
철 산화 방정식.
예를 들어 위의 방정식에서 각 참가자의 NOX를 나타낼 수 있습니다.
시약 철(Fe): 그대로 NOX 0 단체;
시약 내 산소(O): 단순 물질이므로 NOX 0이 있습니다.
제품 내 산소: 알칼리 금속과 결합하지 않아 NOX -2를 함유하고, 알칼리토류 또는 수소 형성 과산화물 또는 과산화물;
제품의 철: 복합 물질이므로 철의 NOX에 2(원자 수)를 곱한 값 + 산소의 NOX에 3을 곱한 값의 합이 0이 되어야 하기 때문에 NOX +3이 있습니다.
x.2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
시약 철(0)과 생성물(+3)의 NOX를 비교하면 증가가 관찰되었습니다. 즉, 다음의 과정을 거쳤습니다. 산화. 의 발생은 주목할 만하다. 산화 예에서 산소에서 발생하는 것처럼 NOx의 감소로 식별되는 환원 현상(전자의 획득을 의미함)이 항상 동반됩니다.
너무 읽기:산화수(NOX) 측정
산화가 발생하는 상황의 예:
1. 연소

물질의 연소는 또한 산화를 나타냅니다.
연소 존재하에서 일어나는 모든 화학반응이다. 연료 모든 산화성 산소 가스(O2) 열과 빛을 생성합니다. 모든 연소 반응에서 발생 산화.
2. 일부 유기 반응
아래 나열된 수단의 존재 하에서 일어나는 모든 유기 반응에서, 산화:
중크롬산칼륨(K2크롬2영형7) 또는 과망간산칼륨(KMnO)4);
강산 또는 강염기의 존재;
오존 가스(O3) 금속성 아연(Zn)과 물(H2영형).
3. 배터리 또는 배터리

배터리는 항상 산화가 일어나는 장치입니다.
스택 또는 배터리는 화학 물질을 저장하는 전기 화학 장치입니다. 이 물질 중 하나는 산화되고 다른 하나는 환원되어 전류가 생성됩니다.
4. 전기분해
전기분해 염을 함유한 수용액에 전류를 가하여 이러한 물질에 존재하는 음이온의 산화를 촉진시키는 화학 공정입니다. 모든 전기분해에는 산화.
By Me 디오고 로페스 디아스
원천: 브라질 학교 - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm
