너 염기성 산화물 그들은 물과 반응할 때 염기를 발생시키는 것들입니다. 산과 반응하면 염과 물을 형성합니다.
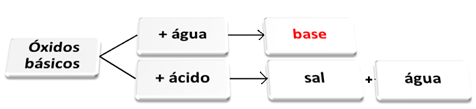
물 및 산과 반응하는 염기성 산화물.
예를 들어 산화나트륨(Na2O), 이는 염기성 산화물이다. 아래에서 물과 반응하면 수산화나트륨 염기를 형성합니다.
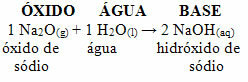
동일한 산화물이 황산(H2오직4), 소금(황산나트륨)과 물이 생성됩니다.
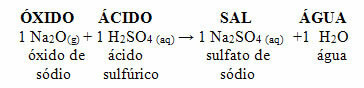
염기성 산화물이 산성 산화물과 반응하면 염도 생성되지만 물은 없습니다.
표시된 예에서 볼 수 있듯이 다른 염기성 산화물도 이온성 화합물이며, 일반적으로 +1과 같은 "전하"를 나타내는 매우 전기양성적인 원소인 금속에 의해 주로 사용됨 또는 +2.
예:
~에2오 = 나1+
케이2오 = K1+
CaO = Ca2+
마그네슘 = 마그네슘2+
이 화합물은 녹는점과 끓는점이 높으며 모두 산소 음이온(O2-).
일부 염기성 산화물의 응용:
• 개: 산화칼슘
이 화합물은 일반적으로 다음과 같이 알려져 있습니다. 생석회. 물과 반응하면 하기 반응에 따라 벽을 칠하는 데 사용되는 염기(수산화칼슘)가 형성되고, 벌레 퇴치, 봉인 보존 및 침투 방지를 주요 목적으로 하는 나무 줄기 및 기타 재료 물에서. 이렇게 형성된 베이스를 수화 석회 따라서 페인트로 칠할 때 이름을 지정합니다. 흰색 페인트.
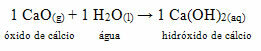

화이트워시 페인팅.
• 케이2영형: 산화칼륨
산화칼륨은 일반적으로 나무와 담배 재에서 발견됩니다. 물과 반응하면 비누 제조에 사용되는 염기성 수산화칼륨(KOH)을 형성합니다. 과거에도 KOH가 없는 곳에서는 K가 함유된 식물성 재를 사용하였다.2O, 지방과 반응하여 소위 말하는 "회색 비누".
제니퍼 포가사
화학과 졸업
원천: 브라질 학교 - https://brasilescola.uol.com.br/quimica/oxidos-basicos.htm
