아미드 카르보닐기(탄소는 산소와 이중 결합을 수행), 질소에 직접 결합되어 차례로 2개의 원자에 결합할 수 있습니다. 수소.
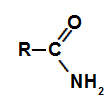
아미드의 관능기
아미드의 분류
a) 단순 아미드
그리고 아마이드 이것은 작용기의 질소에 결합된 두 개의 수소를 가지고 있습니다.

단순 아미드의 구조식
b) 일치환된 아미드
그리고 아마이드 다른 하나는 유기 라디칼로 대체되었기 때문에 작용기의 질소에 결합된 수소는 하나만 있습니다.

일치환 아미드의 구조식
c) 이치환된 아미드
그리고 아마이드 이들은 모두 유기 라디칼로 대체되었기 때문에 관능기 질소에 결합된 수소가 없습니다.

이치환된 아미드의 구조식
아미드의 명명법
다음에 사용해야 하는 IUPAC 명명 규칙 아마이드 é:
접두사 + 중위사 + 아미드
그 중:
접두사: 항상 사슬에 존재하는 탄소의 양과 관련이 있습니다.
중위: 항상 사슬의 탄소 원자 사이의 결합 유형과 관련이 있습니다.
예시:
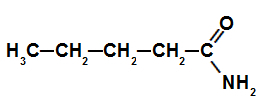
5개의 탄소 원자를 가진 아미드의 구조식
이 예에서 아미드는 5개(펜트 접두사) 탄소 원자와 이러한 탄소 원자 사이에 단일 결합(중위사)만 포함합니다. 그런 이유로 그 이름은 펜타나미드입니다.
만약에 아미드는 분지, 각 급진의 이름과 위치는 합의된 대로 접두사 앞에 기록됩니다. 아래 예를 참고하세요.
예시: 분지형 아미드
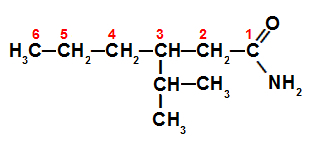
명명법을 위해 구조화된 분지형 아미드
와 같은 아마이드 분지되어 있는 경우, 위에서 번호가 매겨진 주쇄(작용기에서 가장 많은 수의 탄소를 가짐)를 결정하는 것이 필수적입니다. 이 경우 주쇄에는 6개의 탄소(16진 접두사)가 있고 탄소 사이에는 단일 결합(중위)만 있고 탄소 3의 이소프로필 라디칼이 있습니다. 따라서 이 아미드의 이름은 3-이소프로필헥산아미드입니다.
에 일치환 또는 이치환된 아미드, 라디칼이 질소에 직접 연결되어 있으므로 분기의 위치는 항상 N으로 표시됩니다. 체인에 다른 방사형이 있는 경우 N의 라디칼 표시 뒤에 기록됩니다.
예시: 치환된 아미드

명명법을 위해 구조화된 치환된 아미드
이와 같이 아마이드, 치환되는 것 외에도 분지형이므로 주쇄를 결정하는 것이 필수적입니다. 따라서 우리는 6개의 탄소(접두사 16진수), 탄소 사이에 단일 결합(중위)만 있는 주쇄, 탄소 3의 메틸 라디칼 및 질소의 에틸 라디칼을 갖는 주쇄를 갖습니다. 따라서 이 아미드의 이름은 N-에틸-3-메틸헥산아미드입니다.
아미드의 물리적 특성
그들은 물보다 밀도가 낮습니다.
그들은 기본적인 성격을 가지고 있습니다.
특징 극성 분자;
아미드 분자를 함께 유지하는 분자간 힘은 영구 쌍극자;
액체인 메탄아미드를 제외하고 실온에서 고체 상태로 발견됩니다.
탄소 원자가 적을 때 물에 잘 용해됩니다. 그러나 탄소 수가 많을수록 물에 대한 용해도가 낮아지고 유기 용매에 대한 용해도가 높아집니다.
다른 유기 화합물에 비해 녹는점과 끓는점이 높습니다.
아미드의 용도
일반적으로, 아미드 예를 들어 다음과 같이 사용됩니다.
다양한 유기 화합물의 합성(생산)에서;
폭발물 제조;
래커 생산(특정 유형의 수지);
비료 생산에서;
의약품 생산에서;
크림 및 연고 생산.
By Me 디오고 로페스 디아스
원천: 브라질 학교 - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-amidas.htm
