Kps 표현하는 데 사용되는 약어입니다 용해도 곱 상수, 이는의 곱 (곱셈)을 나타냅니다. 물질의 양에있는 농도 용액에 존재하는 이온의.
난 용성 용질이 황산 바륨과 같은 용매에 첨가 될 때마다 소량의 이 소금의 일부는 물에 녹고 나머지는 용기 바닥에 축적되어 배경. 녹는 소금은 고통받습니다 분리, 양이온과 음이온을 물에 방출합니다.

물과 황산 바륨이있는 용액에 침전물이 있음
소금 외에 좋은 선물이 없습니다 용해도, 용해 된 용질의 양은 (용액에 존재하는) 염 이온과 배경 몸체 사이에 용해 평형이 있기 때문에 시간이 지남에 따라 변하지 않습니다.

BaSO 용해 균형4 물 속
용질의 Kps
영형 Kps 용질의 농도는 참여 이온의 몰 농도의 곱입니다. 항상 이온 농도를 각각의 화학 양론 계수 (방정식 균형을 맞추기 위해 사용됨)로 올릴 필요가 있습니다.
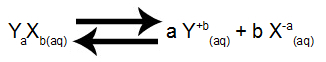
전해질 Y의 용해 평형그만큼엑스비
영형 Kps 소금 Y에 대해 제안 된 평형의그만큼엑스비 시약 Y의 농도 (화학 양 론적 계수 (a)로 증가)와 생성물 X의 농도 (화학 양 론적 계수 (b)로 증가)를 갖게됩니다.
Kps = [Y+b]그만큼.[엑스-그만큼]비
예
물과 시안화 알루미늄 [Al (CN)] 용액을 준비한다고 가정 해 보겠습니다.3], 물에 거의 녹지 않는 소금입니다. 이 소금을 물에 넣으면 해리 현상이 발생합니다.

Al (CN) 전해질 용해 평형3
그래서, 소금 용해 평형 방정식을 통해 우리는 Kps 알루미늄 양이온 (Al+3) 시안화물 음이온 (CN-1) 지수 3으로 올림.
Kps = [Al+3]1. [CN-1]3
용질의 KPS 의미
우리가 찾을 때 Kps 물과 혼합 된 특정 소금의 경우 용액의 각 이온 농도도 알고 있습니다. 이 데이터를 사용하여 용액의 순위 또는 용액에서 용질의 거동을 결정할 수 있습니다. 다음 균형을 고려하십시오.
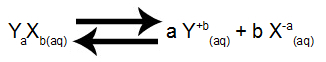
전해질 Y의 용해 평형그만큼엑스비
우리는 다음과 같은 관계를 만들 수 있습니다.
Kps = [Y+b]그만큼.[엑스-그만큼]비 = 0, 침전물이없는 포화 용액이 있습니다.
Kps> [Y+b]그만큼.[엑스-그만큼]비 = 0, 우리는 불포화 용액, 즉 용매에 용해 된 적은 양의 용질을 가지고 있습니다. 용해도 계수);
Kps +b]그만큼.[엑스-그만큼]비 = 0, 우리는 바닥 몸체가있는 포화 용액을 가지고 있습니다. 즉, 전해질 (용질)이 침전 될 것입니다.
전해질의 Kps 값이 너무 낮 으면 용매에 잘 녹지 않는 물질입니다.
의 예 Kps 계산 용질의
(UERN) : 질산 칼슘 [Ca (NO3)2] 물에서 2.0입니다. 10–3 특정 온도에서 mol / liter. 같은 온도에서이 소금의 Kps는 다음과 같습니다.
a) 8.10–8.
b) 8.10–10.
c) 3.2.10–10
d) 3.2.10–8
운동 데이터 :
식염: Ca (NO3)2;
몰염 농도 (용해도): 2.0. 10–3 정부.
Kps를 풀고 계산하려면 다음을 수행해야합니다.
1 단계: 소금 용해 균형을 설정합니다.
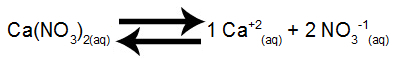
물에서 질산 칼슘 용해 평형
질산 칼슘은 물에서 해리 될 때 1 몰의 칼슘 양이온 (Ca+2) 및 2 mol의 질산염 음이온 (NO3-1).
2 단계: 소금 Kps의 표현을 조립
이 염의 Kps는 아래와 같이 지수 2로 올린 질산 음이온의 농도에 의해 지수 1로 올린 칼슘 양이온 농도의 곱이됩니다.
Kps = [Ca+2]1.[에서3-1]2
3단계: 용액의 이온 농도 값 결정
Kps를 계산하려면 이온 농도 값이 필요하지만 운동은 용액의 소금 몰 농도를 제공했습니다. 각 이온의 농도를 결정하려면 염의 몰 농도에 반응 참여자의 화학 양론 계수를 곱하면됩니다.
칼슘 양이온의 경우 :
[여기+2] = 1. 2,0. 10–3
[여기+2] = 2,0. 10–3 정부
질산 음이온의 경우 :
[에서3-1] = 2. 2,0. 10–3
[에서3-1] = 4,0. 10–3 정부
4단계: Kps 식의 3 단계에서 찾은 농도 값을 사용합니다 (2 단계에서 결정).
Kps = [Ca+2]1.[에서3-1]2
Kps = [2.10-3]1.[4.10-3]2
Kps = 2.10-3.16.10-6
Kps = 32.10-9
또는
Kps = 3.2.10-9 (월 / L)
나로. Diogo Lopes Dias
출처: 브라질 학교- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kps.htm
