분자는 공유 결합으로 연결된 동일하거나 다른 원자의 집합입니다.
이 화학 종은 전기적으로 중성이며 물질의 형성 단위를 나타냅니다.
산소 (O2) 우리가 숨쉬는 공기의. 그러나 다음과 같은 복잡한 화합물도 있습니다. 버키볼 (구 모양으로 결합 된 60 개의 탄소 원자), 이것은 우주에서 지금까지 발견 된 가장 큰 분자입니다.
분자 연구
분자의 공유 결합은 일반적으로 비금속 요소 사이에서 전자를 공유하는 것에 해당합니다.
간단한 화합물의 예로 물 분자를 참조하십시오.
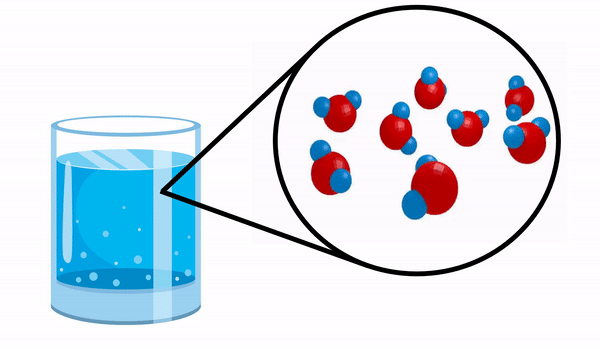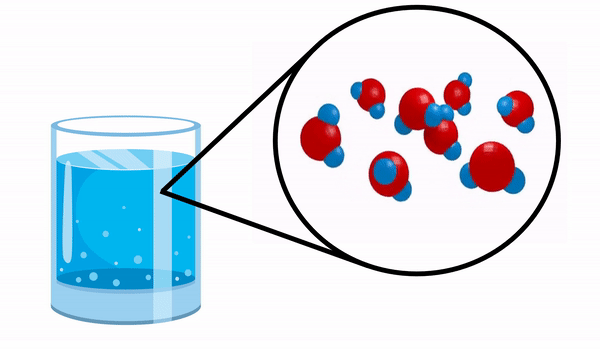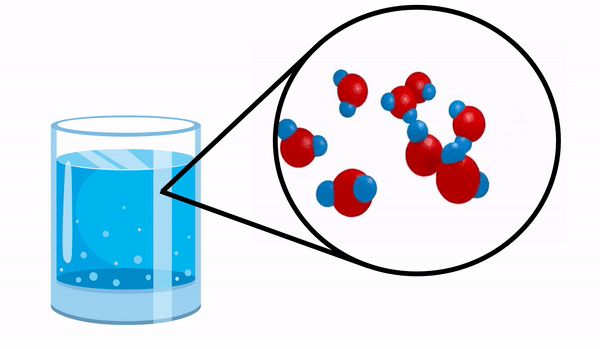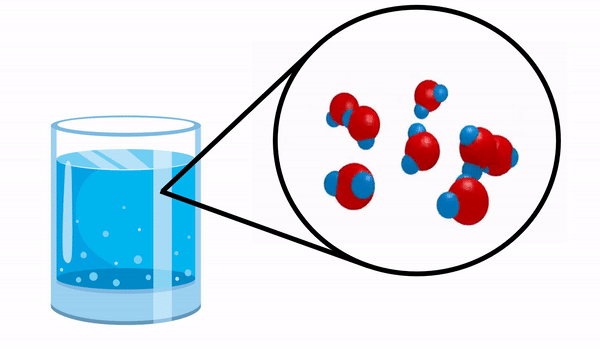
우리가 함께 유리를 관찰 할 때 물 우리는이 물질이 여러 개의 H 분자로 구성되어 있다는 사실을 모릅니다2영형. 이 공식은 물이 서로 전자를 공유하는 2 개의 수소와 1 개의 산소 원자의 3 개의 원자로 구성되어 있음을 나타냅니다.
주스를 달게하고 케이크를 만드는 데 사용하는 설탕도 분자로 이루어져 있습니다. 설탕의 형성 단위는 자당입니다.

이 분자는 훨씬 더 복잡합니다. 원자 연결되었습니다. 그것은 12 개의 탄소 원자, 22 개의 수소 원자 및 11 개의 산소 원자에 의해 형성됩니다.
분자는 알려진 분자 질량의 구조이지만, 너무 많은 원자에 의해 형성된 "거대 구조"인 거대 분자도있어 그 구성이 정의되지 않았습니다. 이 유형의 예는 다이아몬드입니다. 탄소 공유 네트워크에서.
공유 결합
공유 화학 결합은 두 원자가 서로를 공유 할 때 형성됩니다. 전자 더 외부 (가가). 분자는 두 가지 유형의 결합을 가질 수 있습니다.
분자 공유 결합: 두 개의 결합 원자의 전자 쌍이 공유됩니다.

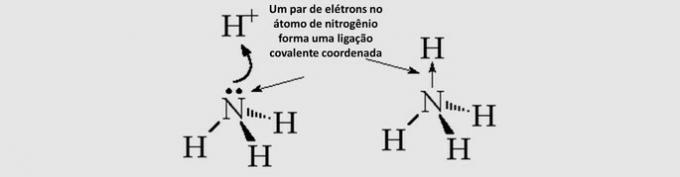
공유 공유 결합 (일수): 공유 전자는 관련된 원자 중 하나에서만 발생합니다.
분자 기하학
분자가 형성 될 때 원자는 다른 방식으로 위치하므로 공간 배열이 더 안정적입니다. 따라서 복합재는 다른 형상을 갖습니다.
다음은 분자가 가질 수있는 몇 가지 기하학입니다.
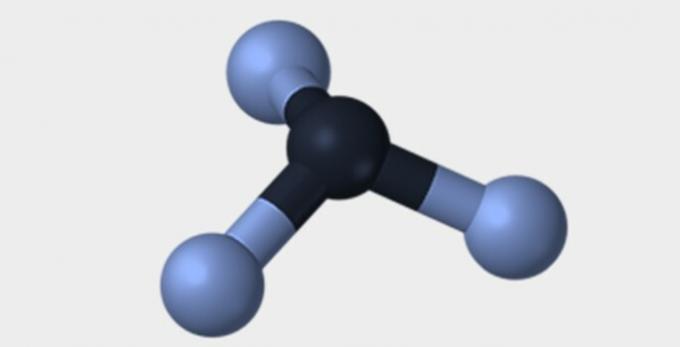
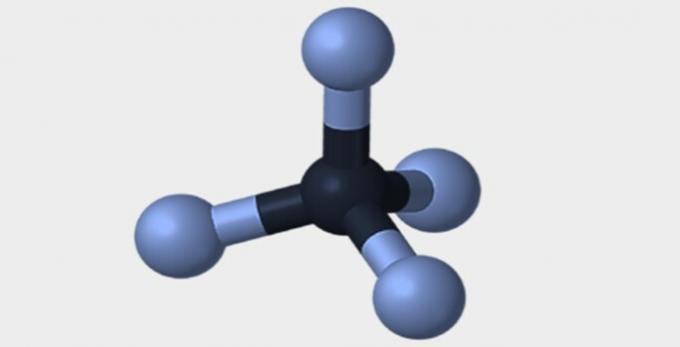
| 분자 기하학 | ||
|---|---|---|
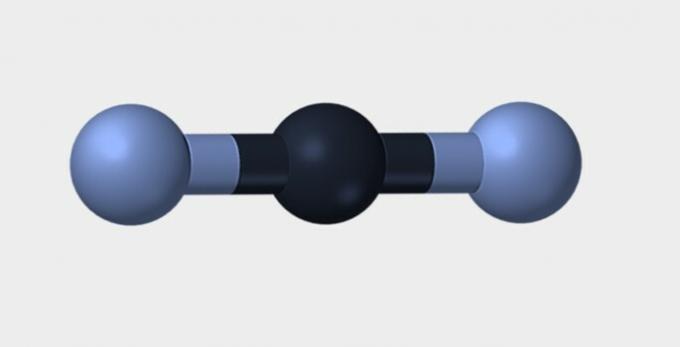
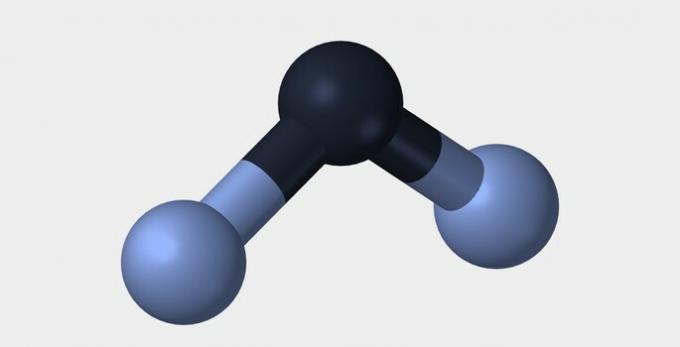
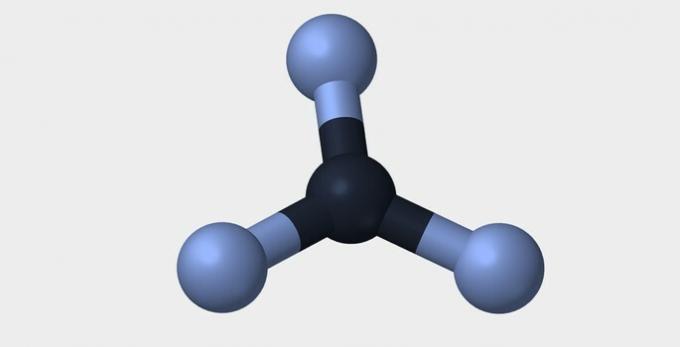
| 선의 | 모난 | 삼각형 |
 |
 |
 |
| 피라미드 | 사면체 | 팔면체 |
 |
 |
 |
극성 및 비극성 분자
분자는 다음에 따라 분류됩니다. 극성.
비극성 분자: 원 자간 전기 음성도 차이가 없습니다.
| 질소 (N2) | 이산화탄소 (CO2) |
|---|---|
 |
 |
질소 (N2)는 비극성 분자입니다. 화학 원소 따라서 전기 음성도에는 차이가 없습니다. 이산화탄소 (CO2)는 선형 기하학으로 인해 비극성이어서 전자에 의한 산소 인력을 안정화시킵니다.
극성 분자: 양극과 음극으로 원자 사이의 전기 음성도 차이가 있습니다.
| 물 (H2영형) | 암모니아 (NH3) |
|---|---|
 |
 |
두 예에서 우리는 중심 원자 인 산소와 질소가 전자 구름을 형성하는 짝을 이루지 않은 전자 쌍을 가지고 있음을 알 수 있습니다. 화학 결합이 확립 된 것보다 중심 원자 주변에 더 많은 전자 구름이 있기 때문에 분자는 극성입니다.
분자의 예
| 물질 | 풍모 | 분자 | 공식 |
|---|---|---|---|
| 수소 | 지각에 연료가 풍부합니다. | 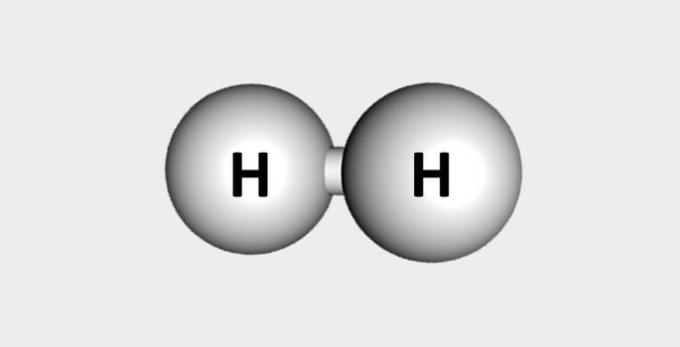 |
H2 |
| 산소 | 호흡에 필수적이며 다양한 화학 반응에 참여 | 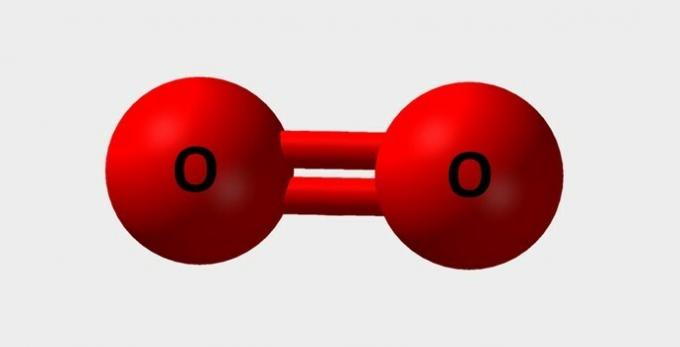 |
영형2 |
| 황 | 염료를 만드는 데 사용되는 노란색 분말. | 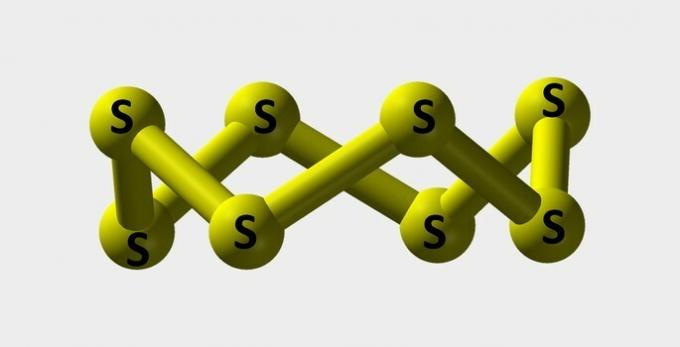 |
에스8 |
| 이산화탄소 | 소화기 및 냉매에 사용됩니다. | 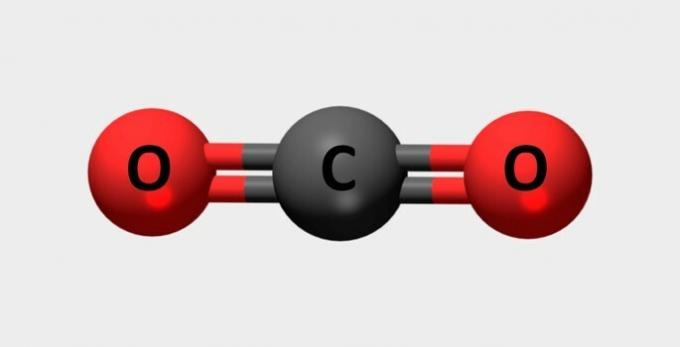 |
CO2 |
| 에탄올 | 연료 및 향수로 사용되는 일반적인 알코올. | 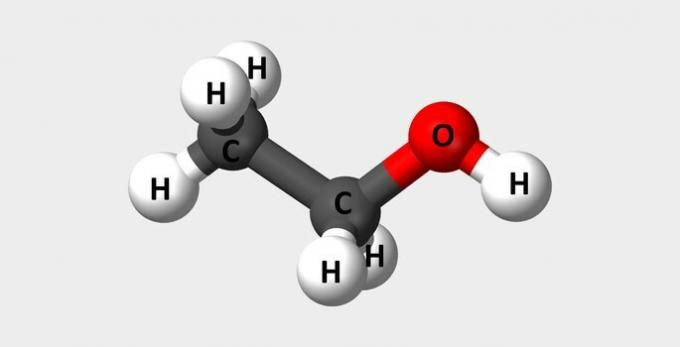 |
씨2H6영형 |
방금 배운 내용과 관련된 주제에 대한 다음 텍스트를 확인하십시오.
- 생체 분자
- 유기 화합물
- 분자 질량
- 옥텟 규칙
- 화학 접착제
- 연결 극성
- 분자간 힘



