* 아 레니 우스 이론 :
수성 매체에서 전기 전도도에 대한 그의 실험을 바탕으로 화학적, 물리적 및 수학적 스웨덴 Svante August Arrhenius (1859-1927)는 1884 년에 다음과 같은 개념을 제안하여 산과 기지 :

따라서 일반적으로 다음이 있습니다.
H+ + H2O → H3영형+
예 :
HCl + H2O → H3영형++ Cl-
HNO3+ H2O → H3영형+ + 아니요3-
H2뿐4+ 2H2O → 2H3영형+ + OS42-

예 :
NaOH → Na + + 오-
Ca (OH)2 → Ca2+ + 2 개 OH-
* Brönsted-Lowry 이론 :
독립적으로 덴마크의 Johannes Nicolaus Brönsted (1879-1947)와 영국의 Thomas Martin Lowry (1874-1936), 같은 해에 Brönsted-Lowry 이론으로 알려진 또 다른 산-염기 이론을 제안했습니다. 수행원:

이 경우 수소 이온은 양성자로 간주됩니다. 이는 다음 반응에서 볼 수 있습니다. 시안화 수소산은 양성자를 물에 제공하여 염기로 작용합니다.
HCN + H2O → CN- + H3영형+
이 반응은 하이드로 늄 이온 (H3영형+) CN 이온에 양성자를 기증 할 수 있음-. 따라서 하이드로 늄 이온 (H3영형+) 산 및 CN으로 작용- 기지로.
CN- + H3영형+→ HCN + H2영형
* 루이스 이론 :
이 이론은 미국의 화학자 Gilbert Newton Lewis (1875-1946)에 의해 만들어졌으며 다음과 같이 말합니다.

이 이론은 새로운 개념을 도입하고 더 포괄적이지만 Brönsted-Lowry 이론을 무효화하지는 않습니다. 모든 루이스 산은 브 뢴스 테드 산이므로 모든 루이스 염기는 브 뢴스 테드 염기입니다. 이것은 양성자가 전자를 받기 때문입니다. 즉, 루이스 산은 루이스 염기에서 고독한 전자 쌍을 연결할 수 있습니다.
루이스에게 산-염기 반응은보다 안정적인 배위 공유 결합의 형성으로 구성됩니다. 따라서 루이스 염기가 한 쌍의 전자를 루이스 염기에 기증하면 둘 다 예에서와 같이 두 전자가 원자 중 하나에서 나오는 배위 공유 결합 소 우는 소리:
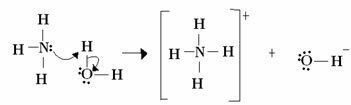
이 경우 암모니아는 두 개의 전자를 양성자에게 제공하고 따라서 양성자를 수용하기 때문에 루이스 및 브 뢴스 테드 염기 역할을합니다. 또한 수소 (양성자)와 암모니아 사이에 공유 결합이 형성되었습니다.
물은 루이스 산과 브 뢴스 테드 산으로 양성자를 제공하고 전자를받습니다. 물에서 생성 된 수산화물의 산소가 어떻게 여분의 전자쌍을 가지고 있는지 주목하세요.

작성자: Jennifer Fogaça
화학 전공
브라질 학교 팀.
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/teorias-acidobase-arrheniusbronstedlowry-lewis.htm
