산화 환원 반응은 원자, 이온 또는 분자 사이의 전자 이동을 포함합니다.
산화-환원 반응에서 산화수 (nox)의 변화가 발생합니다. 산화는 산화 및 환원 과정으로 구성됩니다.
- 산화: 결과 전자 손실 녹스 증가.
- 절감: 결과 전자 이득 녹스 감소.
한 요소가 전자를 포기하면 다른 요소가 전자를받습니다. 따라서 수신 된 총 전자 수는 손실 된 총 전자 수와 같습니다.
연소, 부식 및 광합성에 대한 산화 환원 반응의 예.
예
전자를 받거나 기증하는 요소에 따라 다음과 같은 이름이 있습니다.
- 환원제: 산화 된 것은 환원을 일으키고 녹스가를 증가시킵니다. 그것은 전자를 잃는 것입니다.
- 산화제: 환원을 거쳐 산화를 일으켜 녹스가를 감소시킨 것. 그것은 전자를 얻는 것입니다.
영형 산화수 요소가 참여할 때 요소의 전하를 나타냅니다. 화학 결합.
이 조건은 전기 음성도, 이는 일부 원소가 전자를받는 경향입니다.
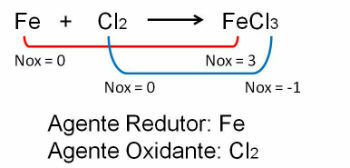
1. 첫 번째 예를 살펴보면 철과 염소 사이의 반응에서 산화수가 변경됩니다. 영형 염소 전기 음성이 더 많기 때문에 전자를 얻습니다.
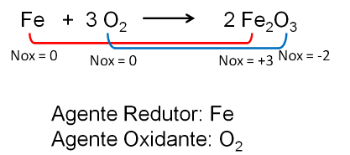
2. 철과 산소의 반응. 산소는 전기 음성이 더 많고 결국 전자를 받아 산화수를 감소시킵니다.
자세한 내용은 다음을 참조하십시오.
- 산화
- 연소
- 화학 반응
- 전자
운동 해결
1. (PUC-RS) 산화 방정식과 관련하여-불균형 환원 Fe0 + CuSO4 → 철2(뿐4)3 + Cu0, 다음과 같이 말할 수 있습니다.
a) 황산구리의 구리 산화수는 +1입니다.
b) 철 원자는 2 개의 전자를 잃는다.
c) 구리는 산화를 겪습니다.
d) 철은 산화제입니다.
e) 철은 산화를 겪습니다.
해결:
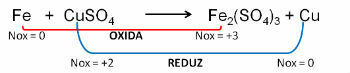
댓글:
e) 철은 산화를 겪습니다.
수업 과정
1. (UFAC-AC) 다음 화학 방정식에서: Zn + 2 HCℓ → ZnCℓ2 + H2
a) 원소 Zn은 산화제로서 산화되고 반응합니다.
b) Zn 원소는 산화되고 환원제로 반응합니다.
c) Zn 원소는 환원제로 환원되고 반응합니다.
d) HCℓ는 환원제입니다.
e) 방정식은 가역적으로 분류됩니다.
b) Zn 원소는 산화되고 환원제로 반응합니다.
2. (ITA-SP) 이온 반응에서 Ni (s) + Cu2+(수성) → Ni2+(수성) + Cu (초)
a) 니켈은 산화되기 때문에 산화제입니다.
b) 니켈은 산화되기 때문에 환원제입니다.
c) 구리 이온은 산화되기 때문에 산화제입니다.
d) 구리 이온은 환원되기 때문에 환원제입니다.
e) 산화 환원 반응이 아니므로 산화제 또는 환원제가 없습니다.
b) 니켈은 산화되기 때문에 환원제입니다.
3. (UFRGS) 가정용 표백제의 활성제는 차아 염소산염 이온 인 ClO-입니다. 표백 공정에서이 이온은 감소합니다. 이는 다음을 의미합니다.
a) 차아 염소산염의 작용을받는 물질은 전자를받습니다.
b) 구조의 전자 수가 감소합니다.
c) ClO-는 환원제입니다.
d) ClO-는 원소 염소 또는 염화물 이온으로 전환됩니다.
e) 전자 이동이 일어나지 않습니다.
d) ClO-는 원소 염소 또는 염화물 이온으로 전환됩니다.