표면 장력은 물과 같은 액체의 표면에 발생하여 박막을 형성하는 현상입니다.
액체 상태의 물이 용기를 차지할 때 우리는 액체와 환경 사이의 분리를 감지할 수 있습니다. 이는 표면의 물 분자 간의 상호 작용이 액체 내부의 상호 작용과 다르기 때문입니다.
표면에서 물 분자는 측면 및 그 아래의 분자와 상호 작용합니다. 내부에는 분자가 다른 분자로 둘러싸여 있으며 수소 결합을 통해 모든 방향으로 상호 작용이 있습니다.
액적 형성 현상을 관찰하는 것은 이 성질 때문이다. 이 때문에 곤충이 물 위를 걷는 것도 가능합니다.
표면장력이란?
그것은 그것을 구성하는 분자 사이의 인력의 불평등으로 인해 액체 아래에 박막이 형성되는 것입니다. 이 현상은 분자간 힘 물처럼 강렬하다.
액체에서 종 사이의 상호 작용을 응집력이라고합니다. 액체 내부의 분자는 모든 방향으로 인접한 분자에 끌리는 반면 표면의 분자는 아래 및 옆에 있는 분자와 상호 작용합니다.
물에서 표면 장력이 어떻게 발생하는지 확인하십시오.
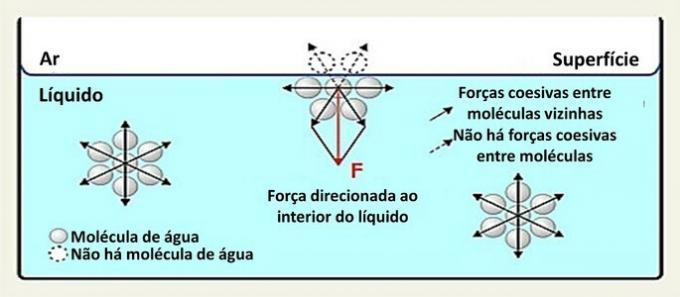
물(H2O)는 2개의 수소 원자(양극)와 1개의 산소 원자(음극)가 결합하여 형성된 극성 분자입니다. 공유 결합. 분자의 양극은 인접한 분자의 음극에 끌어 당겨 수소 결합을 형성합니다.
액체 내에서 이러한 유형의 상호 작용은 모든 방향으로 분산됩니다. 표면에서 힘은 아래쪽과 옆으로 향합니다. 그 위에는 물 분자가 없기 때문입니다. 이것은 표면 분자를 더 응집력있게 만들고 탄성 필름을 만듭니다.
표면 장력 단위는 힘의 단위와 길이의 단위 사이의 몫으로 주어지며 가장 많이 사용되는 것은 다인/센티미터(dyne/cm)와 뉴턴/미터(N/m)입니다.
물은 72.75 dyne/cm의 높은 표면장력을 가지고 있습니다. 그러나 액체 금속인 수은은 표면 장력이 물보다 약 7배 더 큰 475dyne/cm2입니다.
더 알고 싶으십니까? 따라서 다음 텍스트를 확인하십시오.:
- 물 속성
- 극성 및 무극성 분자
- 화학 접착제
표면장력으로 인한 현상
표면 장력은 우리가 일상 생활에서 관찰하는 몇 가지 현상의 원인이 됩니다. 주요 내용은 다음과 같습니다.
물 위를 걷는 동물들

곤충, 거미 및 기타 동물이 걷거나 쉴 수 있습니다. 물 발 끝에는 기름기가 많은 털로 덮여 있어 표면에 붙어 있는 물 분자 사이로 침투할 수 없기 때문이다.
물방울의 형성

물방울은 수축으로 인해 구형이다. 분자 표면 장력으로 인한 표면의. 구는 표면적과 부피 사이의 관계가 가장 작은 기하학적 모양이기 때문에 발생합니다. 따라서 구형은 공기와 접촉하는 물 분자의 수를 가장 적게 유지합니다.
물의 표면 장력 운동
1. 계면 활성제는 다른 물질에 작용하여 변화하는 물질입니다.
a) 삼투압.
b) 표면 장력.
c) 전기 영동.
d) 점도.
e) 삼투압.
올바른 대안: b) 표면 장력.
a) 잘못되었습니다. 삼투압은 주어진 부피의 용매에 포함된 용질 입자의 양과 관련이 있습니다.
b) 정확하다. 세제와 비누는 모두 물의 표면장력을 낮추어 일반적으로 계면활성제는 이러한 물질의 분자가 물 분자 사이에 위치하여 장력을 감소시키기 때문입니다. 피상적.
c) 틀렸다. 전기 영동은 전하에 따라 분자를 분리하는 기술입니다.
d) 잘못되었습니다. 점도는 흐름에 대한 유체의 저항을 결정하는 물리적 특성입니다.
e) 틀렸다. 삼투압은 삼투압이 자발적으로 발생하는 것을 방지하기 위해 시스템에 가해야 하는 압력에 해당하는 집합적 속성입니다.
이 문제에서 다루는 문제에 대해 자세히 알아보기:
- 물질 속성
- Colligative 특성
- 삼투압
2. 액체의 표면 장력은 예를 들어 수소 결합과 같은 분자 간의 상호 작용 과정에 직접적으로 의존합니다. 다음 중 표면 장력이 가장 높은 물질은 무엇입니까?
가) 벤젠
b) 옥탄
c) 에틸 알코올
d) 사염화탄소
e) 에탄올 산
올바른 대안: e) 에탄올 산.
a) 잘못되었습니다. 벤젠은 탄화수소, 비극성 분자이며 수소 결합을 만들지 않습니다.
b) 틀렸다. 옥탄은 탄화수소이므로 수소 결합을하지 않는 비극성 분자입니다.
c) 틀렸다. 에틸 알코올은 수소 결합을 형성할 수 있는 약간 극성인 화합물이지만 분자 간의 상호 작용은 제한적입니다.
d) 잘못되었습니다. 사염화탄소는 비극성 유기 화합물이므로 수소 결합을하지 않습니다.
e) 정답. 카르 복실 산 작용기 (-COOH)는 산소 또는 하이드 록실 수소와 수소 결합을 만들 수 있습니다.

이 문제에서 다루는 문제에 대해 자세히 알아보기:
- 분자의 극성
- 유기적 기능
- 탄화수소
표면 장력 실험
물의 표면 장력을 보여주는 실험으로 아래 비디오를 시청하십시오.

