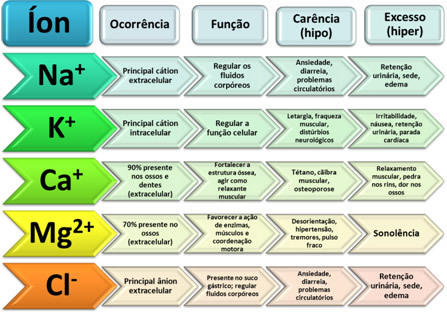
중화 반응은 산이 염기와 반응하여 물과 소금을 형성 할 때 발생합니다. 산은 H 이온을 제공합니다+ 염기는 OH 이온을 제공합니다.- 물 (H2영형):
1 시간+(여기) + 1 개 OH-(여기) → H2영형(ℓ)
이러한 유형의 반응은 매체의 pH가 중화되기 때문에 "중화"라고합니다. 물의 pH는 7.0 (중성)입니다.
이러한 반응이 일어나기 위해서는 에너지의 일부로서 일정량의 열을 방출 할 필요가 있습니다. 이온은 물 분자를 생성하는 결합을 형성하는 데 사용되며 나머지 에너지는 아주. 이 방출 된 에너지를 중화 엔탈피 (∆H중립화).

지금 멈추지 마세요... 광고 후 더 있습니다;)
열을 방출하기 때문에 엔탈피 (시스템의 전체 에너지)가 항상 0보다 작은 음이되는 발열 반응에 해당합니다.
강산과 강염기 사이의 반응의 경우 중화 엔탈피 값은 항상 – 13.8 kcal / mol 또는 – 57.7 kJ / mol입니다. 이것은 염기와 강산이 용액에서 완전히 해리되기 때문에 발생합니다. 열의 발현을 담당하는 반응은 아래 세 가지 예와 같이 물의 형성입니다.
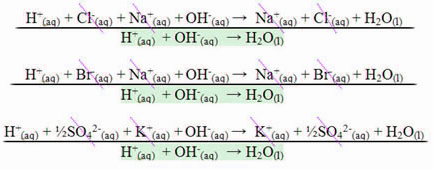
약산 또는 염기와 관련된 중화 반응의 경우 중화 엔탈피 값은 –57.7 kJ / mol 미만입니다.
작성자: Jennifer Fogaça
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "중화의 엔탈피"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm. 2021 년 6 월 28 일 액세스.