"물질의 극성과 용해도 사이의 관계"텍스트에서 일반적으로 용질이 극성 물질은 극성이있는 용매에 용해되고 비극성 물질도 용매에 용해됩니다. 비극성. 그러나 이것은 모든 용해도 케이스에 적용 할 수있는 규칙은 아닙니다.
예를 들어 설탕은 물에 녹지 만 기름은 녹지 않습니다. 물과 설탕 분자는 극성이고 기름 분자는 비극성이지만 분리 된 물질의 분자와 이에 대한 설명을 제공하는 서로 간의 분자간 힘 것.

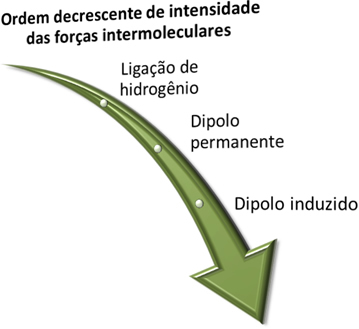
이러한 힘이 무엇인지 알아보기 전에 강도의 문제로 더 강한 수소 결합, 영구 쌍극자 힘이 뒤 따르고 가장 약한 것은 유도 쌍극자 힘입니다.
물과 설탕 분자 (자당-C12H22영형11), 산소 원자가 수소 원자에 결합되어 그룹 ─ O ─ H를 형성합니다. 이것은 물 분자와 설탕 분자 사이에는 분자간 수소 결합 상호 작용이있을 수 있습니다..
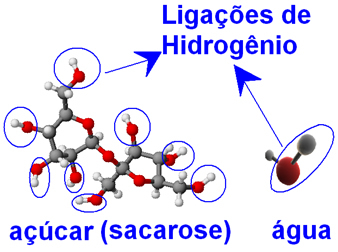
그래서 물 분자가 결정의 형태로 단단히 결합 된 당 분자를 감싸고 분리하여 다시 결합하지 못하게 할 수 있습니다. 따라서 설탕은 물에 잘 녹으며 20ºC에서 100g의 물에 33g까지 녹일 수 있습니다.
이제 기름과 물은 섞이지 않습니다. 이것은 기름이 물에 끌리지 않는다는 것을 의미하지 않습니다. 모양이 아닌 물 표면에 퍼진다는 사실입니다. 구형은 더 많은 양의 오일 분자가 오일 분자와 접촉하는 모양을 찾고 있음을 보여줍니다. 물.
지금 멈추지 마세요... 광고 후 더 있습니다;)
하나, 물 분자 사이의 인력은 기름과 물 분자 사이의 인력보다 훨씬 큽니다 (수소 결합). 따라서 오일 분자는 인접한 두 물 분자 사이의 결합을 끊을 수 없습니다.
이것은 다음과 같은 결론으로 이어집니다.
“기존 분자간 힘이 가능한 새로운 상호 작용보다 더 강하면 용질이 용해되지 않고 원래의 결합이 남아 있습니다. 그러나 새로운 상호 작용이 더 강하면 용질이 용해되어 물질의 분자간 결합이 끊어집니다.”
물질의 용해도에 대한 분자간 힘의 중요성을 보여주는 또 다른 예는 요오드, 물 및 벤젠이있을 때입니다. 아래 다이어그램에서 우리는 요오드가 벤젠에 잘 용해되고 물, 물 및 벤젠에 약간 용해된다는 것을 알 수 있습니다. 완전히 섞이지 않으며 벤젠과 물의 혼합물이 있고 요오드를 첨가하면 벤젠:
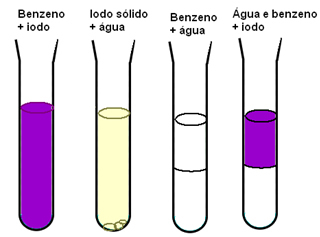
벤젠과 요오드는 비극성으로 극성 인 물보다 혼합 시간이 더 쉽습니다. 그러나 실제로 일어나는 일을 설명하는 것은 비극성 분자 사이에 존재하는 분자간 유도 쌍극자 힘이 물의 수소 결합에 비해 약하다는 것입니다.
따라서 물 분자 간의 기존 상호 작용이 가능한 새로운 상호 작용보다 강하기 때문에 상호 작용, 수소 결합이 끊어지지 않고 벤젠과 혼합시 2 상 시스템이 관찰됩니다. 물.
요오드 분자와 벤젠 분자 사이에 형성되는 새로운 상호 작용은 이러한 분리 된 물질의 분자 사이에서 발생하는 상호 작용보다 더 강합니다.
작성자: Jennifer Fogaça
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "분자간 강도와 물질 용해도의 관계"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/relacao-entre-forca-intermolecular-solubilidade-das-substancias.htm. 2021 년 6 월 27 일 액세스.

