베이스 이다 무기물 스웨덴 화학자에 따르면 스 반테 아 레니 우스, 물에 넣을 때의 현상을 겪습니다 이온 해리, 릴리스가있는 이온: 양이온 (Y+) 및 수산화 음이온 (OH-).

Arrhenius 염기의 일반 공식
a의 Y 그룹 베이스 그것은 모든 금속 또는 암모늄 그룹 (NH4+)는 해리 과정에서 양이온으로 물에서 방출되며, 과정을 나타내는 방정식에서 볼 수 있습니다.
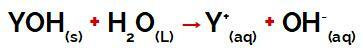
염기의 해리를 나타내는 방정식
분류 및 명명법에 관한 매우 중요한 정보는 아래를 참조하십시오. 기지.
1) 염기 용해도(능력 녹이기 위해 물에)
베이스 녹는: 조성물에 알칼리 금속 또는 암모늄이 있음;
-
베이스 난 용성:있다 알칼리 토금속 구성에서. 예: 제산제 및 완하제로 널리 사용되는 수산화 마그네슘;
지금 멈추지 마세요... 광고 후 더 있습니다;)
실질적으로 기지 불용성: 구성에 다른 금속이 있습니다. 예: 제산제로 널리 사용되는 수산화 알루미늄.
2) 풀뿌리 힘(능력 해리하다 물에)
베이스 강한: 조성에 마그네슘을 제외한 알칼리 또는 알칼리 토금속이 있음;
베이스 약한: 구성에 다른 금속이 있습니다.
3) 기본 명명법
기본 이름을 지정하려면 아래 이름 지정 규칙을 따르십시오.
수산화물 + de + 금속 또는 암모늄의 이름
예: Ca (OH)2 → 수산화칼슘
염기에 IA, IIA 또는 IIIA 계열에 속하지 않는 화학 원소가있는 경우 (그리고 은 또는 아연), 요소 이름 앞에 로마 숫자로 숫자를 표시해야합니다. 수산기 :
예: Ti (OH)4 → 수산화 티탄 IV
나. Diogo Lopes
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
일, Diogo Lopes. "베이스는 무엇입니까?"; 브라질 학교. 가능: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-base.htm. 2021 년 6 월 27 일 액세스.
기본 명명법, 수용액, 이온 해리, 양이온, 음이온, 수산화 나트륨, 수산화 알루미늄, 수산화철, 수산화 구리, 수산화철, 수산화칼슘.