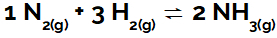그만큼 결합 에너지 관련된다 휴식 시간에또는훈련 중 분자 원자 사이의 하나 이상의 결합. 예를 들어 수소 가스 분자는 관련된 원자 사이에 단일 결합 (시그마)을 가지고 있습니다.

수소 가스 구조식
이 분자가 시작되기 위해 원자 사이에 단일 결합이 형성되었습니다. 이 분자가 염소 가스 (Cl)와 화학 반응에 참여할 때2), 예를 들어 염산 (HCl)의 형성을 위해 H에 존재하는 단일 결합2 그리고 Cl2 결과적으로 HCl에서 단일 결합이 형성되어 끊어 져야합니다.
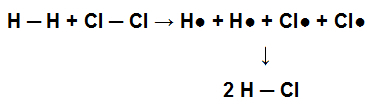
시약에서 단일 결합이 끊어지고 제품에서 단일 결합이 형성되는 것을 나타냅니다.
원자는 서로 결합하여 전자 안정성즉, 그들은 높은 에너지 상황에서 낮은 에너지 상황으로 이동합니다. 따라서 원자 사이의 결합이 형성되면 에너지가 방출된다고 말할 수 있습니다. 따라서 결과적으로 그 분해는 에너지 흡수에 달려 있습니다.
우리가 그것을 이해한다면 헤어짐 화학 결합의 (단선) 공급시 발생 에너지 량 (xKcal), 우리는 이것이 프로세스라는 결론을 내 렸습니다. 흡열. 대조적으로, 유대를 형성하는 것은 해제 준다 같은 양의 에너지 (-xkcal), 존재, 프로세스 발열의.
처럼 화학 반응은 다음과 같이 분류됩니다. 흡열 또는 발열, 우리는 반응물과 생성물 분자의 결합 에너지에 대한 지식을 사용하여 화학 공정의 에너지 변화 (ΔH)를 결정한 다음이를 분류 할 수 있습니다.
예를 들어, 아래 방정식을 참조하십시오.
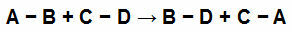
화학 방정식에서 참가자의 화학 결합
각 반응 참가자에는 간단한 링크가 있습니다. 값은 다음과 같습니다.
[A-B] = 50Kcal
[CD] = 100Kcal
[B-D] = 80Kcal
[기원전] = 230Kcal
위의 값을 사용하여 반응물의 결합을 끊고 제품의 결합을 형성하는 데 관련된 에너지를 다음과 같이 계산할 수 있습니다.
시약에서
AB 결합을 끊는 데 50Kcal 과 CD 결합을 끊는 데 100Kcal즉, 시약에서 결합을 끊기 위해 150 Kcal이 사용됩니다.
제품에서
BD 결합을 형성하는 데 80Kcal, AC 결합을 형성하는 데 230Kcal즉, 채권 형성시 제품에서 310 Kcal이 방출됩니다.
반응물 및 생성물에 포함 된 에너지의 값을 통해 반응이 흡수되었는지 또는 흡수되었는지 여부를 알 수 있습니다. 더 많은 에너지를 방출하는 에너지에서 중단에 사용 된 에너지를 빼면 형성:
ΔH = 시약 에너지-제품 에너지
Δ높이 = 230-310
ΔH = -80Kcal
지금 멈추지 마세요... 광고 후 더 있습니다;)
반응이 흡수보다 에너지를 더 많이 방출하므로 음의 ΔH는 발열 성이 있습니다.
노트: 참가자의 화학 양론 계수가 1과 다르면 연결의 에너지 값에 계수를 곱해야합니다. 예를 들면 다음과 같습니다.
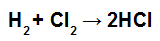
HCl 형성 방정식
HCl의 계수가 2이므로 HCl의 결합 값에 2를 곱해야합니다.
이제 화학 반응에서 결합 에너지에 대한 운동의 해결책을 따르십시오.
예: 다음과 같은 결합 에너지가 주어지면 결합 몰당 킬로 줄 (절대 값) :
고-고 = 436
N ≡ N = 945.6
N − H = 391
열을 계산합니다 (NH 1 몰당 킬로 줄).3 (g)) 다음으로 표시되는 반응에 관여합니다.
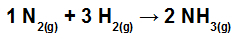
NH 형성 반응의 화학 결합3
해결:
이 연습 문제를 해결하는 첫 번째 단계는 각 분자에 존재하는 화학 결합을 보여주는 방정식을 다시 작성하는 것입니다.
N 없음2: 우리는 삼중 결합을 가지고 있습니다 (왜냐하면 질소의 가족 인 N은 원자가 껍질에 5 개의 전자를 가지고 있기 때문에 3 개의 결합을 만들어야하기 때문입니다).
H에서2: 우리는 단일 결합을 가지고 있습니다 (왜냐하면 H는 원자가 껍질에 전자가 하나만 있기 때문에 하나의 결합 만 만들어야하기 때문입니다).
NH에서3: 우리는 3 개의 단순한 결합이 있습니다 (각 H는 결합이 필요하고 N은 3 개의 결합이 필요하기 때문입니다).
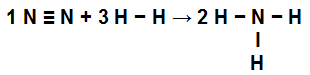
NH 형성의 링크를 보여주는 방정식3
연습이 각 결합에 대한 값을 제공 했으므로 첫 번째 단계는 각 참가자와 관련된 결합 에너지를 결정하는 것입니다.
-N으로2
우리는 1 몰 에 엔2방정식에서 연결을 끊으려면 945.4 KJ가 필요합니다.
1.945,4 = 945.4 킬로그램
-H로2
우리는 3 몰 에 H2방정식에서 연결을 끊으려면 436 KJ가 필요합니다.
3.346 = 1038 KJ
-NH로3
우리는 NH 2 몰3방정식에서, 그러나 N-H 결합은 3 배이므로 결합을 형성하는 데 필요한 에너지의 양에 2와 3을 곱해 봅시다.
2.3.391 = 2346 KJ
마지막으로, 제품을 형성 할 때 방출되는 에너지에서 반응물을 분해하는 데 사용되는 에너지를 빼서 반응에 포함 된 열을 결정할 수 있습니다.
ΔH = 반응물의 에너지-제품의 에너지
Δ고 = (945.4 + 1038)-2346
ΔH = 1983.4-2346
ΔH =-NH 1 몰당 362.6 KJ3 (g)
변동이 음수 였기 때문에 생성물의 결합 형성에서 방출되는 에너지가 반응물의 결합을 끊을 때 흡수 된 에너지보다 더 크다는 것을 의미합니다. 반응은 발열이다.
나. Diogo Lopes Dias