효소 주어진 화학 반응의 속도를 높이는 생물학적 촉매제입니다. 효소는 일반적으로 단백질,하지만 일부 리보 핵산 리보 자임이라고 불리는 효소 역할을합니다.
반응 속도를 높이려면 효소가 기질이라고 알려진 시약에 결합해야합니다. 오랫동안이 링크는 키 잠금 (key-lock)으로 알려진 패턴 인 매우 단단한 것으로 여겨졌습니다. 현재, 그러나, 유도 피팅으로 알려진 모델이 허용됩니다., 기질이 활성 부위로 들어갈 때 효소의 형태에 약간의 변화가 발생한다고 가정합니다.
읽기: 신진 대사는 무엇입니까?
효소 란?
효소는 촉매 역할을하는 생체 분자입니다. 속도를 가속화 할 수있는 물질 화학 반응 이러한 반응 중에 소비되지 않고 살아있는 존재에서 발생합니다. 효소의 작용이 없으면 일부 반응은 매우 느려 신진 대사에 해를 끼칩니다. 효소는 선택적으로 반응을 가속화하므로 매우 특정한 촉매입니다.
효소는 활성화 에너지를 줄임으로써 반응 속도를 높일 수 있습니다. 즉, 반응을 시작하기 위해 추가해야하는 에너지의 양을 줄입니다.
[출판 _ 옴니아]
모든 효소가 단백질입니까?
그들은 종종 단백질 특성의 생물학적 촉매로 정의되지만 모든 효소가 단백질은 아닙니다. 리보 자임이라고하는 효소처럼 기능하는 RNA가 있습니다. 그러나 대부분의 효소는 단백질이므로 아미노산. 이러한 생체 분자의 아미노산 구성은 획득 할 3 차원 구조를 정의합니다.
읽기: 촉매 물질은 어떻게 작용합니까?
효소 기질 복합체
효소가 작용하는 시약 기질이라고합니다. 효소가 기질에 결합하면 복합체가 형성됩니다. 효소 기질. 이 바인딩은 활성 사이트라고하는 특정 영역에서 발생합니다.
단백질 기반 효소에 대해 이야기 할 때 활성 부위는 몇 개의 아미노산에 해당하며 나머지 분자는 활성 부위의 구성을 결정하는 역할을합니다. 활성 부위의 모양과 기질의 모양은 상보 적이어야하므로 효소의 특이성과 관련이 있습니다.
키 잠금 모델
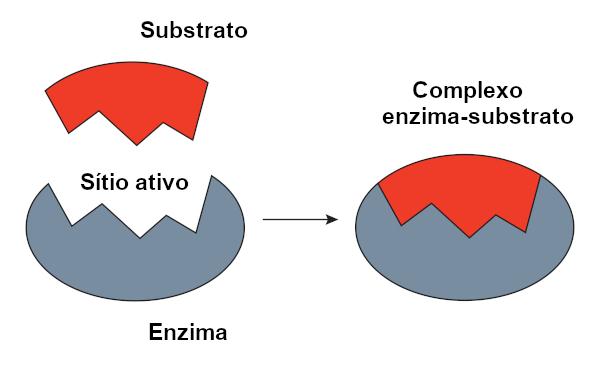
영형 키 잠금 모델Emil Fischer가 제안한는 효소와 기질 간의 상호 작용을 설명하는 데 널리 사용됩니다. 이 모델에 따르면 효소와 기질 사이에는 열쇠와 자물쇠처럼 단단한 상보성이 있습니다. 효소의 활성 부위는 완벽하게 맞는 기질에 대한 보완적인 모양을 가질 것입니다. 따라서 다른 분자는 효소의 특이성을 보장하는이 부위에 접근 할 수 없습니다. 열쇠가 자물쇠 만 여는 것처럼 효소는 기질에만 결합합니다. 그러나 오늘날 우리는 이것이
모델이 올바르지 않습니다, 효소는 이전에 생각했던 것처럼 단단한 구조가 아니기 때문입니다.유도 피팅 모델
현재 효소와 기질 사이의 연관성을 설명하기 위해 가장 많이 사용되는 모델 다음 중 하나입니다 스냅 유도, Koshland et al. 활성 부위와 기질은 열쇠와 자물쇠처럼 단단하게 작동하지 않습니다. 연구에 따르면 기질이 활성 부위로 들어가면 효소가 약간의 변형을 거쳐 활성 부위와 기질 사이에 적합합니다. 이 모델을 더 잘 이해하기 위해 효소와 기질 상호 작용을 악수로 생각할 수 있으며, 이는 첫 번째 접촉 후 더욱 단단해집니다.
보조 인자
대부분의 효소는 보조인 자라고하는 촉매 작용을 수행하기 위해 보조 분자가 필요합니다. 보조인자는 효소에 영구적으로 부착되거나 기질에 약하고 가역적으로 부착 될 수 있습니다. 그들 또한 무기 또는 유기 일 수 있음. 보조 인자가 유기 분자 인 경우 코엔자임.
약간 비타민 예를 들어 비타민 B2라고도 알려진 리보플라빈의 경우가 여기에 해당됩니다. 무기 보조 인자의 예로서 이온 형태의 철과 아연을 언급 할 수 있습니다.
읽기: B 복합 비타민 — 일반적으로 코엔자임 역할을하는 비타민 그룹
효소 분류
효소는 다음과 같이 분류 할 수 있습니다. 여섯 그룹, 그들이 촉매하는 반응 유형을 기준으로 사용합니다.
옥시도 환원 효소: 반응과 관련된 효소 황소절감.
전이 : 한 화합물에서 다른 화합물로의 그룹 이동을 촉매합니다.
가수 분해 효소 : 가수 분해 반응을 촉매합니다.
리스: 이중 결합에 그룹을 추가하거나 이중 결합을 형성하는 그룹을 제거하여 작동합니다.
이성화 효소 : 이성 질화 반응을 촉매합니다.
연결: 분자의 분해를 일으키는 효소 ATP,이 반응에서 방출 된 에너지를 사용하여 새로운 화합물을 형성합니다.
이제 멈추지 마... 광고 후 더 있습니다 ;)
효소 활동을 조절하는 요인
효소의 활성은 요인에 의해 영향을받습니다. 주요 요인은 온도와 pH. 온도는 일반적으로 화학 반응에서 긍정적 인 역할을하여 효소 반응 속도를 증가시킵니다. 그러나 온도 최적 조건 이상으로 증가하면 반응 속도가 상당히 떨어집니다. 단백질의 변성이 관찰되기 때문입니다. 대부분의 인간 효소의 최적 온도는 35 ~ 40 ° C입니다. 온도 외에도 pH 또한 효소 활동에 영향을 미치며 최적의 값도 있습니다. 대부분의 효소에서 최적 pH 값은 6 ~ 8 범위입니다.
작성자: Vanessa Sardinha dos Santos
생물학 교사

