분자간 힘 이들은 공유 결합에 의해 형성된 화합물 분자 (극성 또는 비극성)가 서로 상호 작용하는 방식입니다. 그것들은 네덜란드의 화학자이자 물리학자인 Diderik Van der Waals가 1873 년에 제안했습니다.
Van der Waals에 따르면 분자는 서로 다르게 상호 작용할 수 있습니다. 이러한 다양한 상호 작용은 융점 (MP) 및 비등점 (PE) 물질의. 따라서 분자가 상호 작용하는 강도는 물리적 상태 (고체, 액체 또는 기체).
서로 다른 분자간 힘 (상호 작용)의 존재를 인식하는 것은 간단합니다. 본질적으로 우리는 서로 다른 물리적 상태에서 동일한 물질을 찾을 수 있기 때문입니다. 공유 결합에 의해 형성된 물질 사이에 존재할 수있는 세 가지 유형의 분자간 힘에 대해 알아보십시오.
→ 런던 힘 또는 쌍극자 유도
그것은 사이에서 발생하는 종류의 힘입니다. 비극성 분자즉, 아래 이미지와 같이 전자가 전기 권에 고르게 분포되어 있기 때문에 극 (양극 및 음극)이없는 분자입니다.
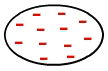
비극성 분자에서 전자의 균일 한 분포
그러나 어떤 지점에서 전자는 분자의 한 영역에 축적되어 그 안에 음극과 양극을 생성 할 수 있습니다. 이 분자가 다른 분자에 가까우므로이 임시 쌍극자는 결국 다른 분자의 전자가 한쪽 끝에서 함께 뭉치도록 유도합니다.

비극성 분자에서 임시 쌍극자의 형성
따라서 비극성 분자는 이제 유도 된 쌍극자를가집니다.
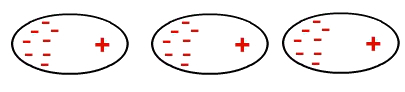
비극성 분자의 상호 작용은 유도
이러한 유형의 힘에 의해 분자가 상호 작용하는 물질의 예는 다음과 같습니다. 이산화탄소 (CO2), 메탄 가스 (CH4), 에탄 가스 (C2H6) 및 수소 가스 (H2).
이제 멈추지 마... 광고 후 더 있습니다 ;)
→ 영구 쌍극자 또는 쌍극자-쌍극자 강도
그것은 사이에 발생하는 일종의 분자간 힘입니다. 극성 분자 (불소, 산소 또는 질소에 직접 연결된 수소 원소를 가진 것 제외). 분자가 쌍극자 쌍극자에 의해 상호 작용하는 물질의 몇 가지 예는 다음과 같습니다. 염산 (HCl), 이산화황 (SO2), 브롬화 수소산 (HBr) 및 시안화 수소산 (HCN).
분자가 극성이기 때문에 (양극과 음극이 있음) 한 쪽의 음극이 다른 쪽의 양극과 결합되도록 상호 작용합니다.
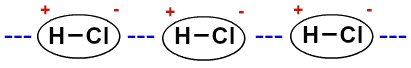
염산 분자 사이의 영구 쌍극자의 표현
쌍극자의 존재로 인해 분자가 극성이기 때문에 쌍극자-쌍극자 상호 작용이 유도 된 쌍극자보다 더 강합니다.
→ 수소 결합
그것은 또한 발생하는 분자간 힘의 유형입니다 극성 분자그러나 수소 원자가 세 가지 화학 원소 (불소, 산소 및 질소) 중 하나에 직접 연결된 경우에만 전기 음성 주기율표의.
수소 결합에 의해 상호 작용하는 분자의 예는 다음과 같습니다: 플루오르 화 수소산 (HF), 암모니아 (NH3) 및 물 (H2영형).
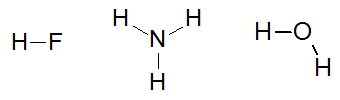
구조식 물질 불산, 암모니아 및 물
원자 간의 전기 음성도 차이가 매우 큰 분자에서 수소 결합이 발생하는 방법 큰, 그것은 고강도 분자간 힘 (쌍극자 쌍극자 및 쌍극자 쌍극자보다 큽니다) 유도).
이 상호 작용의 표현을 참조하십시오.
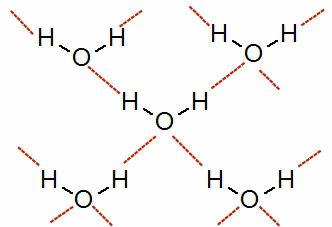
물 분자 사이의 수소 결합 표현
나. Diogo Lopes Dias
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
일, Diogo Lopes. "분자간 힘이란 무엇입니까?"; 브라질 학교. 가능: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-forcas-intermoleculares.htm. 2021 년 6 월 28 일 액세스.

