스포츠 활동, 병원 및 일상 생활에서 고온 및 저온 인스턴트 압축 사용은 매우 일반적입니다. 두 경우 모두 특정 물질이 물과 반응합니다. 예를 들어 냉찜질의 경우 NH에서 물을 분리하는 두 개의 캡슐이 포함되어 있습니다.4에서3, 물에 용해되면 열을 흡수하고 즉석에서 추위를 생성합니다. 뜨거운 압축의 경우 CaCl은 물에 용해됩니다.2 또는 MgSO4, 열을 생성하는 에너지를 방출합니다.
그러나 특정 용액이 발열하여 발열하는 이유; 그리고 다른 사람들은 흡열 성입니까?
이 문제를 이해하려면 솔루션의 엔탈피 변화 (ΔH), 두 단계로 구성됩니다.
(1 차) 망상 엔탈피 (ΔHret): 용질이 물에 녹을 때 첫 번째 단계는 결정 격자에있는 이온을 분리하는 것입니다. 이온 사이의 결합을 끊으려면 시스템에 에너지를 공급해야합니다. 그래서이 첫 번째 과정은 흡열, 에너지를 흡수하므로; 너의 것 양의 엔탈피 (ΔH> 0).
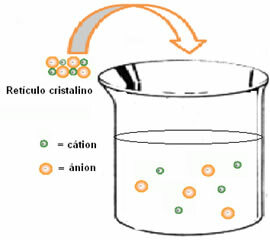
(2 차) 수화 엔탈피 (ΔH숨겼다): 이온이 분리 된 후에는 용매 분자로 둘러싸여 있습니다. 물의 경우 용제이고 수화가 일어나고 있다고 말합니다. 물의 쌍극자는 각각 반대로 하전 된 이온에 끌립니다. 따라서 이러한 상호 작용이 일어나기 위해서는 에너지 방출이 필요합니다. 따라서 수화 엔탈피는 음수가됩니다 (ΔH <0), 프로세스가 발열 성의.
지금 멈추지 마세요... 광고 후 더 있습니다;)
아래 그림은 이온-쌍극자 상호 작용, 즉 분리 된 이온의 전하와 물 쌍극자 사이의 인력이있는 수화가 발생하는 방식을 보여줍니다.
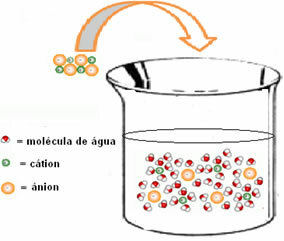
용액의 엔탈피 변화 (ΔH태양)는이 두 엔탈피의 합에 의해 결정됩니다. 결과가 양성이면 망상 엔탈피가 더 높으므로 용해 엔탈피는 프로세스가 흡열임을 나타냅니다.
흡열 용해의 엔탈피 다이어그램은 다음과 같습니다.
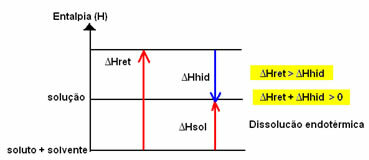
이것은 아래에 표시된 요오드화 칼륨 용해의 경우로 표시됩니다.
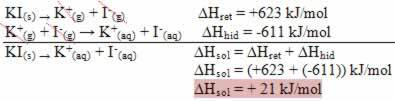
엔탈피 다이어그램은 다음과 같이 표시됩니다.
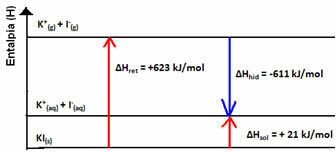
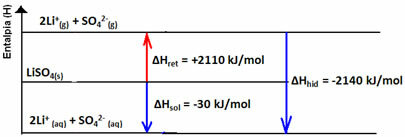
결과가 양성이면 수화 엔탈피가 망상 엔탈피보다 크고 과정은 발열입니다. 발열 용해의 엔탈피 다이어그램은 다음 예와 같이 표시됩니다.
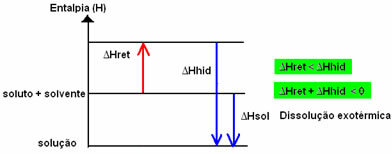
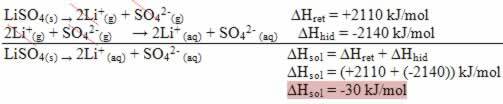
아래의 엔탈피 다이어그램을 참고하십시오.
작성자: Jennifer Fogaça
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "솔루션 엔탈피 변형"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/variacao-entalpia-solucao.htm. 2021 년 6 월 28 일 액세스.