그만큼 편평한 또는 헌법 적 이성질체 둘 이상의 화합물이 동일한 분자식을 갖지만 구조가 일부 측면에서 다른 하나입니다. 이러한 측면 중 하나는 불포화, 기능 및 분기의 위치.
그래서 우리는 위치 또는 위치 이성질체 이는 이성질체가 동일한 탄소 사슬을 가지지 만 언급 된 요인 중 하나의 위치에 따라 다를 때 발생합니다.
첫 번째 예 :불포화 위치
아래의 두 화합물은 동일한 분자식 C를 가지고 있습니다.5H10그러나 그 불포화 (이중 결합)는 각 경우에 서로 다른 탄소 사이에서 발견됩니다. 첫 번째 분자에서 이중 결합은 탄소 1과 2 사이에 있고, 두 번째 분자에서는 탄소 2와 3 사이에 있습니다.
H2씨 ═CH CH2CH2CH3 H3씨 CH2CH ═CH CH3
갇힌-1-참여-2-아니
두 번째 예 :기능의 위치
다음으로 우리는 동일한 분자식 C를 갖는 동일한 기능 (케톤)을 갖는 두 개의 이성질체를 가지고 있습니다.6H12그러나 작용기 (카르 보닐)의 위치는 다릅니다. 첫 번째로 카르 보닐은 탄소 2를 남기고 있습니다. 다른 화합물에서는 탄소 3을 남깁니다.
영형영형
║║
H3씨 ─ 씨CH2CH2CH2CH3 H3씨 CH2─ 씨CH2CH2CH3
헥산2-한 헥산-3-하나
지금 멈추지 마세요... 광고 후 더 있습니다;)
위치 이성질체에서 모든 이성질체는 동일한 화학적 기능에 속한다는 것을 기억하는 것이 중요합니다.
세 번째 예 :지점 위치
아래의 두 화합물은 모두 분자식 C를 갖습니다.7H16그러나 첫 번째 화합물의 (메틸) 가지가 탄소 2에서 나오고 있습니다. 두 번째 화합물에서는 탄소 3에 있습니다.
H3C ─ CH CH2 CH2 CH2 CH3 H3C CH2 ─ CH CH2 CH2 CH3
||
CH3CH3
2- 메틸-헥산 3- 메틸-헥산
노트 : 특별한 유형의 위치 이성질체도 있지만 이것은 별도로 고려됩니다. 그녀는 불린다 나는보상 합계 또는 메타 메리아, 그 차이는 헤테로 원자 (탄소 사이의 탄소 사슬에 나타나는 원자)의 위치에 있기 때문입니다.
예: H3C ─ 영형 CH2 CH2 CH2 CH3 H3C CH2 ─ 영형 CH2 CH2 CH3
작성자: Jennifer Fogaça
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "위치 이성질체"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/isomeria-posicao.htm. 2021 년 6 월 27 일에 액세스했습니다.
화학
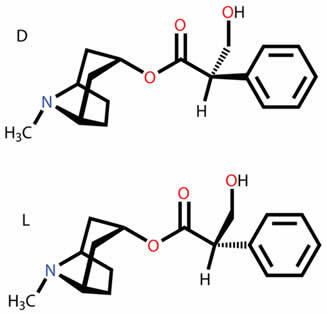
기능, 위치, 사슬, 호 변이성, 메타 머리 즘, 시스-트랜스 기하 및 광학 이성체와 같은 다양한 유형의 평면 및 공간 이성체가 무엇인지 알아 봅니다.