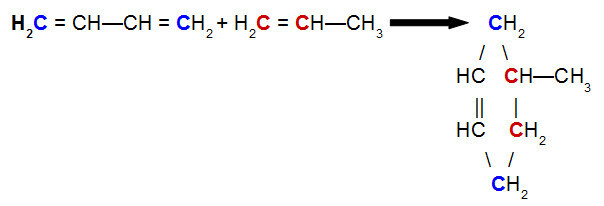산 산화물은 물과 반응 할 때 산을 제품으로 생성하는 산화물입니다. 염기와 반응 할 때 제품은 소금과 물이됩니다.
이러한 화합물은 일반적으로 공유 특성을 가지고 있습니다. 즉, 분자이고 물에 용해되며 대부분 높은 전기 음성도를 가진 원소 인 비금속에 의해 형성됩니다. 금속에 의해 형성되면 산화수 (전하)가 높습니다.
예 :
CO2, 뿐2, 뿐3, P2영형5, Cl2영형6, 에서2, 아니2영형4, 아니2영형5등
다음은 산 산화물에 대한 특성 반응의 일반적인 계획과 예입니다.
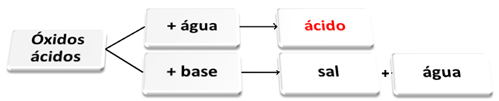
물 및 염기와 반응하는 산성 산화물
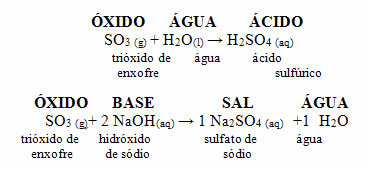
산성 산화물은 또한 무수물,이 단어는 그리스어에서 왔기 때문입니다. 무수물, 즉 "물 없음", 산 산화물은 "무 수산"으로 간주 될 수 있습니다.
일부 산 산화물의 특성 및 응용 :
• 이산화탄소 (이산화탄소)-CO2:
이 화합물은 높은 압력을 받으면 물에 용해되기 때문에 청량 음료와 미네랄 워터의 가스로 사용됩니다. 아래 반응에 따라 물과 반응하여 산을 생성하는 산성 산화물이기 때문에 이러한 제품에서 산성 매질을 생성합니다.

78 ° C 이하에서는 고체 상태로 드라이 아이스로 불리며 외관이 얼음을 닮았 기 때문에 이름이 붙여졌습니다. 일반적이지만 녹지 않고 실온에서 액체 상태로 전달되지만 증기 상태, 즉 승화. 따라서이 기능은 콘서트, 영화, 극장, 파티 등에서 경치 좋은 자원으로 사용됩니다.

이산화탄소는 산성 산화물입니다
또한 인간의 호흡, 화석 연료 (석탄, 석유 제품, 알코올 등)의 연소 및 산불의 결과로 대기에서 발견됩니다. 따라서 그는 산성비를 담당하는 사람 중 한 명입니다.
지금 멈추지 마세요... 광고 후 더 있습니다;)
• 황산화물-SO2 그리고 그래서3
이 산화물은 대기 중에도 존재하며 자연적이고 인공적인 기원을 가지고 있습니다. 자연은 화산 폭발과 식물과 동물의 분해를 통해 발생합니다. 인공물은 대기 중 가장 많은 양의 산화물에 해당합니다. 화석 연료, 주로 디젤 유를 태워서 배출되며 불결.
이산화황 (SO2) 대기 중의 산소와 반응하여 삼산화황 (SO3). 이 마지막 산화물이 빗물과 반응하면 황산이 생성되어 매우 강하고 손상을 입 힙니다.
• 연료에서 연소하는 유황: S + O2 → OS2
• SO2를 SO3로 변환: SO2 + ½2 → OS3
SO2 및 SO3와 물과의 반응으로 산: SO2 + H2O → H2뿐3
뿐3 + H2O → H2뿐4
• 사산 화이 질소 (무수 질소)-N2영형4
이 화합물은 끓는점이 22ºC이고 노란색을 띠며 매우 휘발성입니다. 그것은 질소의 산화에 의해 대기에서 형성되며 액체 형태, 일산화 질소 또는 산화 질소의 이량 체 (NO2). 그 온도 이상에서는 NO의 형태를 취합니다.2:
엔2영형4 ↔ 아니오2
매우 독성이 강한 가스이며 흡입하면 치명적입니다. 또한 로켓 연료의 구성에도 사용됩니다.
작성자: Jennifer Fogaça
화학 전공