그만큼 먼저법준다열역학 응용 프로그램입니다 원리준다보존준다에너지 열역학 시스템 용. 이 법칙에 따르면 내부 에너지 열역학 시스템의 양 사이의 차이입니다 열 시스템과 시스템에 의해 수행 된 작업에 흡수됩니다.
보기또한:열학의 기본 개념 및 요약
열역학 제 1 법칙은 무엇입니까?
열역학 제 1 법칙은 에너지 보존 원리의 직접적인 결과입니다. 이 원칙에 따르면 시스템의 총 에너지항상 일정하다, 그녀는 잃어버린 것이 아니라 변형되기 때문입니다.
범위 내 열역학, 사용됨 더 구체적인 개념 에너지 절약 원칙에 사용되는 것보다 덜 일반적입니다. 열역학 제 1 법칙에서 우리는 다음과 같은 개념을 사용합니다. 에너지내부의,열 과 작업, 범위와 관련된 열 기계 (열역학에 근본적으로 중요한 기술적 응용).

증기 구동 식 기계를 상상해보십시오. 기계의 작동 유체 (수증기)가 외부 소스로부터 열을 받으면 두 가지 에너지 변환이 가능합니다. 온도 몇도 증가하거나 심지어 넓히다 그 기계의 피스톤을 움직여 일정량의 작업.
"열역학 시스템의 내부 에너지의 변화는 열역학 시스템이 흡수하는 열량과이 시스템이 수행하는 작업량 간의 차이에 해당합니다."
열역학 제 1 법칙의 공식
열역학 제 1 법칙을 수학적으로 설명하는 데 사용되는 공식은 다음과 같습니다.

유 – 내부 에너지 변동 (cal 또는 J)
큐 – 열 (라임 또는 J)
τ – 작업 (라임 또는 J)
이 공식을 사용하려면 몇 가지 신호 규칙에주의해야합니다.
ΔU – 시스템 온도가 상승하면 양수입니다.
ΔU – 시스템 온도가 낮아지면 음수가됩니다.
큐 – 시스템이 외부 환경에서 열을 흡수하면 긍정적입니다.
큐 – 시스템이 외부 환경에 열을 제공하면 음수가됩니다.
τ – 시스템이 확장되어 외부 환경에 대한 작업을 수행하면 긍정적일 것입니다.
τ – 시스템이 계약하면 부정적이며 외부 환경에서 작업을받습니다.
내부 에너지 변동
용어 ΔU는 운동 에너지 시스템의 구성 입자 중 이상 기체의 경우 ΔU는 다음과 같다고 말할 수 있습니다.
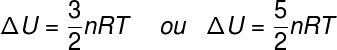
아니 – 몰수 (mol)
아르 자형 – 이상 기체의 보편적 상수 (0.082 atm.l / mol. K 또는 8.31 J / mol. 케이)
티 – 절대 온도 (켈빈)
공식을 분석하면 시스템에 온도 변화가 없으면 내부 에너지 또한 변경되지 않습니다. 또한 주기적으로 작동하는 열 기계의 경우 각주기가 끝날 때 내부 에너지의 변동은 null이어야합니다., 그 시점에서 엔진은 초기 온도로 다시 작동하기 때문입니다.
보기또한:열 기계의 성능: 어떻게 계산합니까?
열
시스템으로 전달되는 열의 양을 나타내는 다음 용어 인 Q로 이동하면 일반적으로 열량계의 기본 방정식, 아래 표시 :
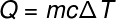
큐 -열 (라임 또는 J)
미디엄 – 질량 (g 또는 kg)
씨 – 비열 (cal / gºC 또는 J / kg. 케이)
ΔT – 온도 변화 (섭씨 또는 켈빈)
작업
열역학 제 1 법칙과 관련된 마지막 양은 일 (τ)입니다. 일정한 압력 하에서 발생하는 변환만을위한 분석 공식, 또한 알려진 처럼 등압 변환, 손목 시계:
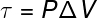
피 – 압력 (Pa 또는 atm)
ΔV – 부피 변화 (m³ 또는 l)
시스템에 가해지는 압력이 일정하지 않으면 압력 대 체적 그래프 영역 (P x V)으로 작업을 계산할 수 있습니다. 이 스칼라 크기에 대해 자세히 알아 보려면 다음을 방문하십시오. 작업.
해결 된 운동
질문 1)(CefetMG) 닫힌 열 사이클에서 수행되는 작업은 100J와 같고 열 교환과 관련된 열은 각각 고온 및 저온 소스에서 1000J와 900J입니다.
열역학 제 1 법칙에서이 열주기의 내부 에너지의 변화는 줄 단위로 다음과 같습니다.
a) 0
b) 100
c) 800
d) 900
e) 1000
해결
대안 a.
열역학 제 1 법칙을 사용하여 문제를 해결해 보겠습니다.

성명서에 따르면 우리는 닫힌 열역학적 사이클에서 내부 에너지의 변화를 계산해야하며, 이 경우 우리는 기계가 사이클 시작시와 동일한 온도에서 작동하기 때문에 내부 에너지 변동은 0이어야합니다.
질문 2)(Upf) 이상 기체의 샘플은 등압 및 단열 변환 중에 부피를 두 배로 늘립니다. 가스가 경험하는 압력이 5.10이라고 생각하면6 Pa 및 초기 볼륨 2.10-5 m³, 다음과 같이 말할 수 있습니다.
a) 공정 중 가스에 의해 흡수되는 열은 25cal입니다.
b) 팽창하는 동안 가스가 수행하는 작업은 100cal입니다.
c) 가스의 내부 에너지 변동은 –100J입니다.
d) 가스 온도가 일정하게 유지됩니다.
e) 해당 사항 없음.
해결
대안 c.
운동 성명서에서 제공하는 정보를 사용하여 올바른 대안을 찾기 위해 열역학 제 1 법칙을 사용할 것입니다.
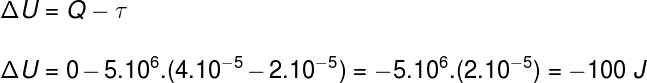
질문 3)(와) 주방 용기에는 고압 가스가 들어 있습니다. 이 실린더를 열면 가스가 빠르게 대기로 빠져 나가는 것을 볼 수 있습니다. 이 과정은 매우 빠르기 때문에 단열 과정이라고 생각할 수 있습니다.
열역학 제 1 법칙이 ΔU = Q-W로 주어 졌다는 것을 고려하면, 여기서 ΔU는 에너지의 변화입니다. 가스 내부에서 Q는 열의 형태로 전달되는 에너지이고 W는 가스가하는 일입니다. 맞습니다. 다음과 같이 진술하십시오.
a) 가스 압력이 증가하고 온도가 감소했습니다.
b) 가스에 의해 수행 된 작업은 양수 였고 가스 온도는 변하지 않았습니다.
c) 가스에 의한 작업은 양수 였고 가스 온도는 감소했습니다.
d) 가스 압력이 증가하고 수행 된 작업이 부정적이었습니다.
해결
대안 c.
가스 부피가 커지면 수행 한 작업이 긍정적이라고, 즉 가스 자체가 외부 환경에서 작업을 수행했다고 말합니다. 또한 공정이 매우 빠르게 진행되기 때문에 가스가 주변과 열을 교환 할 시간이 없으므로 다음과 같은 상황이 발생합니다.
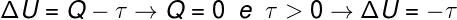
계산에 따르면 가스의 내부 에너지는 수행 한 작업과 동일한 양만큼 감소합니다. 가스에 의해 또한 가스의 내부 에너지가 감소하기 때문에 온도.
질문 4)(Udesc) 물리학 실험실에서는 열역학적 분석 목적을 위해 이상 기체로 간주 될 수있는 기체로 실험이 수행됩니다. 가스가 열역학적 과정을 거친 실험 중 하나를 분석 한 결과, 가스에 공급되는 모든 열이 일로 변환 된 것으로 결론지었습니다.
나타내는 대안을 선택하십시오. 바르게 실험에서 수행 된 열역학적 과정.
a) isovolumetric 프로세스
b) 등온 과정
c) 등압 과정
d) 단열 과정
e) 복합 공정: 등압 및 등압
해결
대안 b.
가스에 공급되는 모든 열이 일로 변환되기 위해서는 내부 에너지의 흡수가 없어야합니다. 즉, 가스는 등온 과정, 즉 온도에서 일어나는 과정을 거쳐야합니다. 일정한.
작성자: Rafael Hellerbrock
물리학 교사
출처: 브라질 학교- https://brasilescola.uol.com.br/fisica/primeira-lei-da-termodinamica.htm

