주로 물리 화학에서 연구되는 산화 환원 반응은 전자 전달이 일어나는 반응이다. 하나 이상의 전자를 잃는 반응 종 (원자, 이온 또는 분자)은 산화를 겪는 종입니다. 반면에 전자를받는 화학 종은 감소합니다.
일반적으로 이러한 유형의 반응을 무기 화학에서 연구하면 간단한 교환 반응 또는 변위.
어떤 반응이 일어나려면 특정 조건을 충족해야합니다. 그들 중 하나는 화학적 친 화성 즉, 새로운 물질의 형성을 가능하게하는 방식으로 상호 작용해야합니다.
산화 환원 반응의 경우 친화 성은 반응물 중 하나가 전자를 얻는 경향이 있고 다른 하나가 전자를 잃는 경향이 있음을 의미합니다. 이 추세는 반동 관련된 화학 원소의.
금속 간의 반응성을 어떻게 비교할 수 있는지 살펴 보겠습니다.
황산구리 (CuSO) 용액을 저장한다고 가정합니다.4). 다음과 같은 반응이 일어나기 때문에이 용액을 알루미늄 용기에 넣을 수 없습니다.
2 Al(에스) + 3 CuSO4 (수성)→ 3 Cu(에스) + Al2(뿐4)3 (수성)
알루미늄은 산화되어 각각 3 개의 전자를 잃고 알루미늄 양이온이됩니다.
Al(에스) → 알3+(여기) + 3 및-
동시에 구리 양이온 (Cu2+) 용액에 존재하는 것은 알루미늄에서 전자를 받아 환원되어 금속 구리가됩니다. 각 구리 양이온은 두 개의 전자를받습니다.
나귀2+(여기) + 2 및- → Cu(에스)
그러나 그 반대의 경우 알루미늄 황산염 (Al2(뿐4)3 (수성)),이 반응이 일어나지 않기 때문에 구리 용기에 넣어도 문제가되지 않습니다.
나귀(에스) + Al2(뿐4)3 (수성) → 발생하지 않습니다
이러한 관찰 된 사실은 다음과 같은 사실로 설명 될 수 있습니다. 알루미늄은 구리보다 반응성이 높습니다..
금속은 전자를 포기하는, 즉 산화하는 경향이 있습니다. 다양한 금속을 비교할 때 전자를 기부하는 경향이 가장 큰 것이 가장 반응성이 높습니다.. 결과적으로 금속의 반응성은 이온화 에너지즉, 기저 상태의 기체 원자에서 전자를 제거하는 데 필요한 최소 에너지입니다.
지금 멈추지 마세요... 광고 후 더 있습니다;)

이를 바탕으로 금속 반응성 큐 또는 전해 전압 행, 아래 표시 :
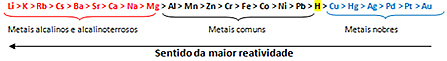
반응성이 가장 높은 금속은 양이온이 덜 반응성 인 이온 물질과 반응합니다. 즉, 왼쪽의 금속은 오른쪽의 이온에 의해 형성된 물질과 반응합니다. 그 반대는 일어나지 않습니다.
주어진 예를 기억하면, 알루미늄 (Al)이 구리 (Cu)의 왼쪽에있는 반응성 행을 참조하십시오. 따라서 알루미늄은 구리 양이온에 의해 형성된 용액과 반응합니다. 그러나 구리는 알루미늄 양이온에 의해 형성된 용액과 반응하지 않습니다.
반응성이 가장 높은 금속은 리튬 (Li)이고 반응성이 가장 낮은 금속은 금 (Au)입니다.

이것이 금이 그토록 가치있는 이유 중 하나입니다. 반응하지 않으면 오랫동안 손상되지 않기 때문입니다. 이것은 금으로 코팅 된 이집트 석관과 가장 먼 고대로 거슬러 올라가는 조각품에서 볼 수 있습니다. 우리는 또한 순금 보석의 내구성을 금보다 반응성이 더 높은 다른 금속으로 만든 보석과 비교할 때 이것을 볼 수 있습니다.

작성자: Jennifer Fogaça
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "금속의 반응성 순서"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-metais.htm. 2021 년 6 월 28 일 액세스.