通常の反応 水性電解 そして 火成電気分解 それらは、反応に関与しないグラファイトおよび白金電極を使用して実行されます。 それらは電流を伝導するだけです。 ただし、使用する必要がある特定のケースがいくつかあります アクティブ電極つまり、還元と酸化を受けます。
レドックスプロセスに関与するこれらの電極の主な使用例は次のとおりです。 電解金属精製、亜鉛、コバルト、ニッケル、特に銅など。 そしてまた 電気めっき. それぞれのケースがどのように発生するかを見てみましょう。
• 銅電解精製:この電解銅精錬は約99.9%の純度を生み出すことができ、主に 不純物が最も少ない銅線は、非常に電流を流す能力がある可能性があります 減少した。
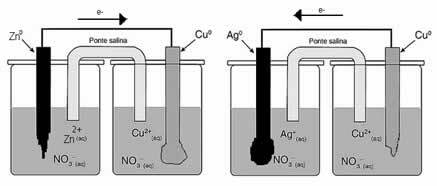
以下に組み立てられた電解槽の概略図を見て、このプロセスがどのように行われるかを観察してください。

硫酸銅水溶液(CuSo4(aq))–電気を通す–不純な金属銅であるアノードは電子を失います。つまり、酸化を受けて陽イオン(Cu)を放出します。2+)、ネガティブプレートに堆積します。 これは、不活性なプラチナプレート、またはより良いのは純銅プレートである可能性があります。 それは陰極を構成し、銅がその中に堆積するにつれて還元されます。 したがって、電極で発生する半反応は次のとおりです。
今やめないで... 広告の後にもっとあります;)
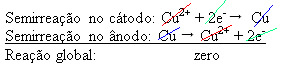
結果がゼロであるという事実は、化学反応がなく、銅の輸送のみがあったことを示しています。 容器の底には、金、銀、シリカ(砂)、その他の鉱物など、銅に含まれていた他の不純な物質があり、販売することもできます。
• 電気めっき:腐食から保護される材料に金属コーティングが施されています。
コーティングに選択された金属-クロム(クロムメッキ)、ニッケル(ニッケルメッキ)、銀(銀メッキ)、 金(金メッキ)または亜鉛(亜鉛メッキ)–陽極、正極になり、酸化を受けて電子を失います。 還元電位が大きいため、保護されている材料の代わりに酸化されます。
負極、つまりこれらの電子を受け取って還元を受ける陰極は、コーティングされた材料そのものです。 このようにして、表面が何らかの形で侵害された場合でも、保護されたままになります。
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "アクティブ電極による電気分解";
ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm. 2021年6月28日にアクセス。