君は 塩一般に、直接的または間接的に、人々の日常生活において非常に重要です。 私たちが家庭で使用する多くの製品には、化学に属するこれらの物質が存在します 無機物、または私たちが持っている他の材料の生産またはケアにさえ関連しています アクセス。
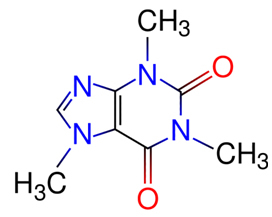
私たちが家庭で消費する処理水はその一例であり、処理中に段階を経て、これらの段階の1つで塩が使用されます。 この目的で使用される塩は硫酸アルミニウムであり、その化学式は次のように表されます。 アル2(のみ4)3, SOグループであること4 と呼ばれる 硫酸塩 とAlは要素のシンボルです アルミニウム.
塩なので、 硫酸アルミニウム この無機グループの他の代表者にもあるいくつかの特徴があります。
イオン性です
苦しむ 解離 水中で
室温で固体です
塩味があります
その特定の機能は次のとおりです。
白です
水に溶け、溶解度は870g / Lです。
770の融点を持っています OÇ
沸点がある:該当なし、
その密度は2.672g / mlです
水と接触すると、それは溶解し、次のプロセスを経ます 解離、次の式で表されます。
アル2(のみ4)3 →2アル+3(ここに) + 3 SO4-2(ここに)
この塩の生産には化学プロセスが含まれます。つまり、その製造は現象に依存します(化学反応)特定の化学物質。 メソッドの取得の2つの例は次のとおりです。
今やめないで... 広告の後にもっとあります;)
中和反応
反応 酸が塩基と反応して塩と水を形成します。 これは、水酸化アルミニウムが硫酸と反応して、硫酸アルミニウムと水を形成するときです。 プロセスを表す方程式は次のとおりです。
3時間2のみ4 + 2 Al(OH)3 →アル2(のみ4)3 + 6 H2O
簡単な交換反応
単体が複合物質と反応する反応。 これを行うために、金属アルミニウムの存在下で硫酸を入れ、硫酸アルミニウムと水素ガスを生成します。
3時間2のみ4 + 2 Al(s)→アル2(のみ4)3 + 6 H2(g)
この塩を知ることの重要性は、それが飲料水処理の凝集プロセスで広く使用されているという事実によるものです。 水中に存在する懸濁液中の固体不純物に付着するという特徴があり、デカンテーションプロセスをより簡単かつ効率的にします。

家庭での硫酸アルミニウムの使用場所
あなたの使用 国内の 主にプールの水を処理するために一部の人々によって行われていますが、家庭での使用は変更することによって避ける必要があります pH 水の量とこの塩が引き起こす可能性があるという事実:
皮膚刺激性
粘膜刺激性
吸入すると気道を火傷する可能性があります
摂取すると、食道や胃などを火傷する可能性があります。
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "硫酸アルミニウム"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/sulfato-aluminio.htm. 2021年6月28日にアクセス。
イオン性化合物、イオン性化合物の主な特徴、イオン間の結合、電子の決定的な移動、 イオン、負イオンと正イオン、陰イオン、陽イオン、イオン結合、分子構造間の静電引力 彼
化学

解離とイオン化、イタリアの科学者ボルタ、電流、スウェーデンの物理化学者Svant August Arrhenius、理論 アレニウス、陽イオン、陽イオン、陰イオン、陰イオン、苛性ソーダ、食塩、極性分子、解離 イオン性、